请用学过的知识分析其中的化学原理并写出化学方程式,属于离子反应的请写出离子方程式。(1)将氯气通入熟石灰即可制的漂白粉【漂白粉的有效成分是次氯酸钙Ca(ClO)2,商品漂白粉往往含有Ca(OH)2等杂质】 。(2)漂白粉之所以具有漂白作用是由于Ca(ClO)2在水溶液中发生水解反应生成具有强氧化性的物质 。(3)Ca(OH)2杂质的存在使溶液的碱性增强,因此漂白作用进行缓慢。要在短时间受到漂白效果,必须除去Ca(OH)2,所以工业上使用漂白粉是常加入少量弱酸如醋酸等,或加入少量的稀盐酸 、
。(4)家庭使用漂白粉不必加酸,因为水中的CO2也起到了弱酸的作用 。(5)不要将漂白粉与洁厕剂等强酸性物质混合使用,因为在强酸性条件下二者可以发生氧化还原反应生成一种有毒气体:
已知Fe(s)+CO2(g) FeO(s)+CO(g) K1…①
FeO(s)+CO(g) K1…①
Fe(s)+H2O(g) FeO(s)+H2(g) K2…②
FeO(s)+H2(g) K2…②
H2(g)+CO2(g) H2O(g)+CO(g) K3…③
H2O(g)+CO(g) K3…③
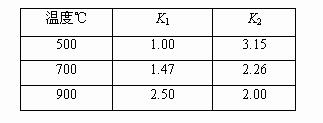
又已知不同温度下,K1、K2值如下:
| 温度℃ |
K1 |
K2 |
| 500 |
1.00 |
3.15 |
| 700 |
1.47 |
2.26 |
| 900 |
2.50 |
2.00 |
| 温度℃ |
K1 |
K2 |
| 500 |
1.00 |
3.15 |
| 700 |
1.47 |
2.26 |
| 900 |
2.50 |
2.00 |
(1)若500℃时进行反应①,CO2起始浓度为1.6 mol·L-1, 4分钟后建立平衡,用CO表示的反应速率为。
(2)900℃ 进行反应③,其平衡常数K3为(求具体数值),焓变ΔH0(填“>”、“=”或“<”),若已知该反应仅在高温时正反应自发,则ΔS0(填“>”、“=”或“<”)。
(3)下列图像符合反应②的是(填序号)(图中v是速率,φ为混合物中H2的体积百分含量)。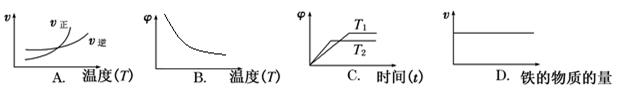
(12分)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中的溶质足量),当闭合该装置的电键K时,观察到电流表的指针发生了偏转。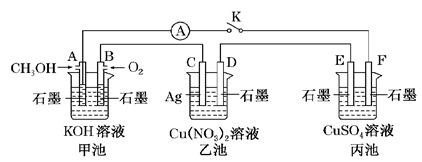
请回答下列问题:
(1)甲池为________(填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为_____________。
(2)丙池中F电极为________(填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为____________________________________________________________。
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为________mL(标准状况)。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是________(填字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(OH)2CO3 |
2SO2(g)+ O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH =" -" 99 kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH =" -" 99 kJ·mol-1
请回答下列问题:
(1)图中A表示_____________________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________。
(2)图中ΔH =" __________" kJ·mol-1。
(3)如果反应速率v(SO2)为0.06 mol·L-1·min-1,则v(O2)为__________ mol·L-1·min-1。
(4)已知S(s) + O2(g) = SO2(g) ΔH =" -" 296 kJ·mol-1,则由S(s)生成5 mol SO3(g)的ΔH=kJ·mol-1。
已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下
3Cu + 8HNO3 ="=" 3Cu(NO3)2 + 2NO↑+ 4H2O
(1)用双线桥法分析上述反应(只需标出电子得失的方向和数目)
3Cu + 8HNO3 ="=" 3Cu(NO3)2 + 2NO↑+ 4H2O
(2)上述反应中氧化剂是,氧化产物是(填化学式)。
(3)若19.2g铜与足量硝酸完全反应,则消耗硝酸为mol,被还原的硝酸为mol,生成NO的体积为L(标准状况) 。
(11分)有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、氯化钡溶液、碳酸钾溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各盛少量多次进行两两混合反应,反应现象为:A与B、A与E产生沉淀,B与D、B与E产生沉淀,C与E、D与E产生气体,而C与D无反应现象。
由此,可判定各试剂瓶中所盛试剂为(写化学式)
A____________、B____________、C、____________、D____________、E____________。
另外,请写出下面要求的离子方程式:
(1)A与E:_______________________________________________________________。
(2)B与E:_______________________________________________________________。
(3)C与E:____________________________________________________________。