A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。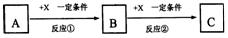
试回答:
(1)若X是强氧化性单质,则A不可能是 。
a、S b、N2 c、Na d、Mg e、Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,
则B的化学式为 ;C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示) ,检验此C溶液中金属元素价态的操作方法是
_____________________________________________________________________________。
(3)若A、B、C为含金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为 ,X的化学式可能为(写出不同类物质) 或 ,反应①的离子方程式为 或 。
某化学兴趣小组为探究SO 2的性质,按下图所示装置进行实验。
(1)装置A中盛放亚硫酸钠的仪器名称是___________,其中发生反应的化学方程式为
________________________________________________________________________;
(2)实验过程中,装置B、C中发生的现象分别是________________、 ________________,
这些现象分别说明SO2具有的性质是_________ ___和____________;装置B中发生反应
的离子方程式为______________________________________。
(3)设计装置D的目的是____________________________________________________。
(4)尾气应用____________________溶液吸收(填试剂的化学式).
A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。E是地壳中含量最高的金属元素。
根据以上信息回答下列问题:
(1)D元素在周期表中的位置是,乙物质的晶体中所含化学键的类型为,阴离子与阳离子的个数比为,其电子式为。
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)。
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是
。
(4)请设计比较D与E金属性强弱的实验方法(简述实验步骤、现象与结论):
。
按要求完成以下方程式:
(1)磁性氧化铁溶于盐酸的化学方程式:_________________________________________。
(2)氯化铁溶液中通入SO2气体的离子方程式:_______________ ____________________。
(3)偏铝酸钠溶液中通入过量CO2的离子方程式:_________________________________。
(4)碳单质和浓硝酸反应的化学方程式:_________________________________________。
现有A、B、C、D、E五种元素,都是短周期元素,其中A、B、C原子序数依次递增并都相差1, B元素原子M层上的电子数和K层上的电子数相同。B单质与D单质反应后可形成化合物BD2;B单质与E单质可形成化合物BE。D的阴离子比B的阳离子多一个电子层,而E阴离子与B的阳离子电子层结构相同。
(1)五种元素的名称是A_______;B______;C_______;D______;E________。
(2)写出A单质在D单质中燃烧的化学方程式:_____________________。
(3)写出A最高价氧化物的水化物的溶液与只由C、E两种元素组成的固体化合物反应的离子方程式:___________________________________________。
在①35Cl、②37Cl—、③12C、④23Na+、⑤24Mg2+、⑥14C中;(用序号回答下列问题)
(1)粒子半径比较:①_____②;④_____⑤(填 < = > 号)
(2)微粒中质子数等于中子数的是____________,核外电子数相等的微粒______ ______;
(3)_________与_________互为同位素,共有___________种元素。