A、B、C、D、E、F是原子序数依次增大的同周期元素,已知A、C、F的原子最外层电子数之和为11,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应,均生成盐和水;D元素原子的次外层电子数比最外层电子数多4,E元素原子的最外层与最内层电子数的差是3。试回答下列问题:
(1)写出下列元素符号:A ,C ,D ,E 。
(2)用电子式表示B和F形成化合物的过程: 。
(3)写出A、C、F三种元素最高价氧化物对应的水化物相互反应的化学方程式:
、 、 。
工业氢氧化钾的溶液中含有某些含氧酸的钾盐杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜,其工作原理如图所示。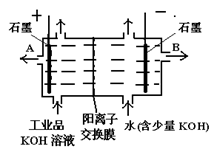
(1)该电解槽的阳极反应式为:
(2)阳离子交换膜的作用是
(3)通电开始后,阴极附近溶液pH会增大,其主要原因是(填序号)
A.阳极区的OH-移向阴极所致
B.阴极产生的金属钾与水反应生成了大量OH-
C.阴极由H2O电离出的H+放电生成H2,促进水的电离,使OH-浓度增大
(4)除去杂质后的氢氧化钾溶液从溶液出口_____________(填写“A”或“B”)导出。
化学在能源开发与利用中起着十分关键的作用。
(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体。甲烷气体燃烧的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ/mol。
356g“可燃冰”(若分子式为CH4·9H2O)释放的甲 烷气体完全燃烧生成液态水.放出的热量为
烷气体完全燃烧生成液态水.放出的热量为
kJ。
(2)Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如右图所示,电解总反应为2Cu+H2O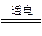 Cu2O+H2
Cu2O+H2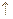 。该电解池中,铜电极接直流电源的极;每生成1molCu2O,电路中通过的电子的数目为;该电解
。该电解池中,铜电极接直流电源的极;每生成1molCu2O,电路中通过的电子的数目为;该电解 池的阴极反应式为。
池的阴极反应式为。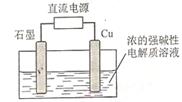
已知A 是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
请回答下列问题:
(1)写出A的结构简式。
(2)B、C分子中的官能团名称分别是、。
(3)写出与E具有相同官能团的D的同分异构体的结构简式。
(4)写出下列反应的化学方程式:
①;反应类型:。
④;反应类型:。
(1)把一块纯净的锌片插入盛有稀硫酸的烧杯里,可观察到锌片逐渐溶解,并有气体产生,再平行地插入一块铜片(如图甲所示),可观察到铜片上(填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来(如图乙所示),可观察到铜片上(填“有”或“没有”)气泡产生。
(2)用导线连接灵敏电流表的两端后,再与溶液中的锌片和铜片相连(如图丙所示),观察到灵敏电流表的指针发生了偏转,说明了导线中有电流通过。图乙、图丙是一个将能转化为能的装置, 人们把它叫做原电池。
人们把它叫做原电池。
(3)从上述现象中可以归纳出构成原电池的一些条件是,有关的电极反应式:锌片;铜片。
用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
(1)实验过 程如下图所示,分析判断________段化学反应速率最快,这段反应速率最快的原因是。
程如下图所示,分析判断________段化学反应速率最快,这段反应速率最快的原因是。
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
| A.蒸馏水 | B.氯化钠固体 | C.氯化钠溶液 | D.浓盐酸 |
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(回答一种即可)
。