苯环上原有的取代基对新导入苯环上的取代基的位置有一定影响,其规律是:
①苯环上新导入的取代基所占的位置主要决定于原有取代基的性质。
②可以把原有取代基分成两类:第一类如:―OH,―X(Cl,Br), ,—R等,可使新导入的取代基进入苯环的邻位和对位;第二类如—NO2、—SO3H、—CHO等,可使新导入的取代基进入苯环的间位。当第一类和第二类同时存在时,以第一类为准。
,—R等,可使新导入的取代基进入苯环的邻位和对位;第二类如—NO2、—SO3H、—CHO等,可使新导入的取代基进入苯环的间位。当第一类和第二类同时存在时,以第一类为准。
(1)请写出图中第②步反应的化学方程式及C的结构简式。
②的化学方程式是 。
(2)C的结构简式为 。
(3)写出同分异构体D,E的结构简式:D ;E 。
电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过“中温焙烧—钠氧化法”回收Na2Cr2O7等物质。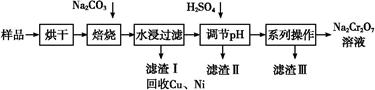
已知:在Na2CrO4溶液中含有少量NaAlO2、Na2ZnO2等物质
(1)水浸后的溶液呈 性(填“酸”、“碱”或“中”)。
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式。
Cr(OH)3+ Na2CO3+ 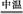 Na2CrO4+ CO2+
Na2CrO4+ CO2+
(3)滤渣Ⅱ的主要成分有Zn(OH)2、 。
(4)“系列操作”中为:继续加入H2SO4, ,冷却结晶,过滤。继续加入H2SO4目的是 。
已知:①除去滤渣II后,溶液中存在如下反应:
2CrO42—+2H+ Cr2O72—+H2O
Cr2O72—+H2O
②Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表
| 温度 溶解度 化学式 |
20 ℃ |
60 ℃ |
100 ℃ |
| Na2SO4 |
19.5 |
45.3 |
42.5 |
| Na2Cr2O7 |
183 |
269 |
415 |
| Na2CrO4 |
84 |
115 |
126 |
(5)工业上还可以在水浸过滤后的溶液(Na2CrO4)加入适量H2SO4,用石墨作电极电解生产金属铬,写出生成铬的电极反应方程式 。
材料是人类生存和发展的重要物质基础,随着科学技术的发展,人们使用材料的种类、数量和质量也不断的发展,生产、生活的条件和质量也发生了巨大的变化。
(1)无机非金属材料包括传统无机非金属材料和无机非金属新材料,下列属于无机非金属新材料的是 (多选,选填字母代号)。
a.复合材料 b.单晶硅 c.金刚石 d.石墨e.C60 f.玻璃
(2)北京奥运会撑杆跳项目中运动员使用的撑杆材料是复合材料。这种材料由 和增强体两部分组成,其中增强体的作用是 。
(3)玻璃和水泥是两种用途极为广泛的材料。工业制备这两种材料使用的共同原料是 。
(4)铁是重要的金属材料,工业上一般用石灰石、 、 和空气在 (填写工业生产设备名称)中炼制生铁。
(5)合成高分子材料的小分子叫 。
锆产业是极有发展潜力及前景的新兴产业,锆(Zr)元素是核反应堆燃料棒的包裹材料,二氧化锆(ZrO2)可以制造耐高温纳米陶瓷。我国有丰富的锆英石(ZrSiO4),含Al2O3、SiO2、Fe2O3等杂质,生产锆流程之一如下:
试回答下列问题:
(1)写出上述流程中高温气化的反应方程式(碳转化成CO):;
(2)写出ZrOCl2·8H2O在900 ℃生成ZrO2的反应方程式 ;
(3)关于二氧化锆纳米陶瓷和锆合金的说法不正确的是 (单选)。
| A.二氧化锆纳米陶瓷是新型无机非金属材料 |
| B.1纳米=10-10米 |
| C.锆合金的硬度比纯锆要高 |
| D.日本福岛核电站的爆炸可能是由锆合金在高温下与水蒸气反应产生的氢气爆炸引起 |
我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如图
(1)上述生产纯碱的方法称 ,副产品的一种用途为 。
(2)沉淀池中发生的化学反应方程式是 。
(3)写出上述流程中X物质的分子式 。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了 (填上述流程中的编号)的循环。从沉淀池中取出沉淀的操作是 。
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加 。
(6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有 。
a.增大NH4+的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
南海某小岛上,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示水的硬度为28°(属于硬水),主要含钙离子、镁离子、氯离子和硫酸根离子。请思考下列问题:
(1)该泉水属于 硬水(填写“暂时”或“永久”)。
(2)若要除去Ca2+、Mg2+可以往水中加入石灰和纯碱,试剂添加时先加 后加 ,原因是。
(3)目前常用阳离子交换树脂如NaR、HR来进行水的软化,若使用HR作为阳离子交换树脂则水中的Ca2+、Mg2+与交换树脂的 起离子交换作用。若使用NaR作为阳离子交换树脂失效后可放入5%-8% 溶液中再生。
(4)岛上还可以用海水淡化来获得淡水。下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42—等离子,电极为惰性电极。请分析下列问题:
①阳离子交换膜是指 (填A或B)。
②写出通电后阳极区的电极反应式:;阴极区的现象是: 。