N2H4(联氨又称肼)一种无色发烟的、具有腐蚀性和强还原性的无色油状液体,它是一种重要的化工试剂,在生产和生活中有着重要的作用。
(1)推测有关N2H4的性质,下列说法正确的是
| A.具有高度吸湿性、可燃性 |
| B.有微弱的氨味,与甲醇,乙醇互溶,但不溶于乙醚、氯仿和苯 |
| C.N2H4的水溶液呈弱碱性, |
| D.联氨的水溶液既有氧化性又有还原性,酸性溶液以氧化性为主,还原产物是N2,碱性溶液以还原性为主,氧化产物是NH4+ |
E.高温加热时分解为氮气、氢气和氨气。
(2)请写出N2H5+的电子式:__________________________
(3)在高锰酸钾催化剂存在下,尿素(CO(NH2)2)和次氯酸钠-氢氧化钠溶液反应制得联氨,它和水能按任意比例互相混溶,形成稳定的水合肼N2H4·H2O写出反应的离子方程式:______________________
(4)发射卫星可用肼为燃料,用NO2作氧化剂,二者发生反应生成氮气和水蒸气。已知:
N2(g)+2O2(g)=2NO2 (g) H=+67.7kJ•mol-1,N2H4(g)+O2(g)=N2(g)+2H2O(g) H=-534kJ•mol-1,
写出气态肼和NO2反应的热化学方程式__________。
(5)肼--空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,负极电极反应式是____________________________
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,1mol该配合物能与3molAgNO3恰好完全沉淀 。请用对应的相关元素的化学用语规范填空:
(1)A、B、C的第一电离能由小到大的顺序为___________________________。
(2)B的氢化物(B2H4)的分子中心原子采取_______杂化。
(3)写出化合物AC2的电子式________________;一种由B、C组成的化合物与AC2互为等电子体,其化学式为____________________。
(4)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学
方程式是(并标出双线桥表示电子转移的方向和数目)。
(5)E3+的核外电子排布式是______________,ECl3形成的配合物的化学式为___________。
碳化硅(SiC) 、氧化铝(Al2O3) 和氮化硅(Si3N4)是优良的高温结构陶瓷,在工业生产和科技领域有重要用途。宇宙火箭和导弹中,大量用钛代替钢铁。
(1)Al的离子结构示意图为;
Al与NaOH溶液反应的离子方程式为
(2)氮化硅抗腐蚀能力很强,但易被氢氟酸腐蚀,氮化硅与氢氟酸反应生成四氟化硅和一种铵盐,
其反应方程式为
(3)工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g) + x N2(g) + 6 H2(g) Si3N4(s) + 12 HCl(g) △H<0
Si3N4(s) + 12 HCl(g) △H<0
在恒温、恒容时,分别将0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2 L密闭容器内,进行上述反应,5 min达到平衡状态,所得HCl(g)为0.3mol/L、 N2为0.05 mol/L
① H2的平均反应速率是
② 反应前与达到平衡时容器内的压强之比=
③ 系数 x =
(4)已知:TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g) ΔH1=+140 kJ·mol-1
C(s)+ O2(g)=== CO(g) ΔH2 =-110 kJ·mol-1
O2(g)=== CO(g) ΔH2 =-110 kJ·mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:
。
A、B、C三元素原子的核外电子数都比氩原子少, A和C处于同主族, 两
者间隔一周期, A元素和B元素的原子两者核电荷数之差为5, B原子核外M层比L层少2个电子, 则:
(1)B原子的电子式为__________;A离子的结构示意图为_____________。
(2)C原子核里含有一个中子的原子的符号为_________,用电子式表示A与B所形成化合物的形成过程 。
(3)A元素在周期表中的位置为_____________________。
下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝,X分解产生A、B、C三种产物的比值为1:1:1。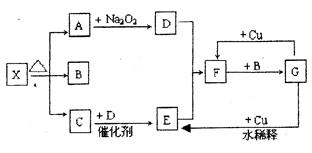
(1)写出下列各物质的化学式:
X:;B:;F:;G:。
(2)按要求写出下列变化的反应化学方程式:
A→D的化学反应方程式:;
G→E的离子反应方程式:。
下表是元素周期表的前三周期,针对表中A~G七种元素填空:
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 |
A |
|||||||
| 2 |
B |
C |
D |
|||||
| 3 |
E |
F |
G |
(1)A、B两种元素组成相对分子质量最小的化合物,其分子的空间结构为。
(2)七种元素中的最高价氧化物对应水化物的酸性最强的是(用化学式表示,下同);碱性最强的是,该化合物属于。(选填离子或共价化合物),该化合物的电子式为,所含化学键类有、。
(3)用A、D的单质可以制成燃料电池,电池中装有E的最高价氧化物的水化物的浓溶液作电解质溶液,用多孔的金属惰性电极浸入上述浓溶液中,在X极通入D的单质,Y极通入A的单质,则Y极是该电池的极(选填正极或者负极),X极的电极反应式是。当电池中转移1mol 电子时,消耗A单质的体积为L(标况)。