t℃时,将3mol A和1mol B气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g) xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol·L—1,请填写下列空白:
xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol·L—1,请填写下列空白:
(1)从开始反应至达到平衡状态,生成B的平均反应速率为 。
(2)x= ,平衡常数K= 。
( 3)若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母) 。
3)若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母) 。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(4)若向原平衡混合物的容器中再充入a mol C,在t℃时达到新的平衡,此时B的物质的量为n(B)= mol。
(5)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应该满足的关系式为 。
(15分)本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做一题。若两题都作答,则以A题计分。
A.《化学与生活》
(1)良好的生态环境可以提升生活质量。
①空气质量报告的各项指标可以反映出各地的空气质量。下列各项中目前未列入我国空气质量报告的是(选填字母,下同)。
a.SO2
b.NO2
c.CO2
d.PM2.5
e.氯氟烃
②垃圾应分类收集。以下物质应放置于贴有“ ”标志垃圾筒的是。
”标志垃圾筒的是。
a.废电池b.废铝制的易拉罐c.建筑固弃物、渣土
③近日,公安机关成功破获了一起特大利用“地沟油”制售食用油案件。综合利用“地沟油”的一种方法,通常将“地沟油”进行简单加工提纯后,水解分离可获取和(填名称)。
(2)人体健康与食品、药物等关系密切。
①合理搭配饮食是我们的健康理念。比如早餐搭配:牛奶、面包、黄油、水果等,其中含有的营养素有油脂、糖类、、、无机盐和水。
②生活中应合理地摄取人体必需的元素,体内元素含量过高或过低,会引起甲状腺疾病;当人体内缺钙时,可能患有的疾病是。
a.贫血b.骨质疏松 c.夜盲症
③氢氧化铝可以用来治疗胃酸过多,请写出该反应的离子方程式。
④青霉素适合治疗的疾病是。
a.感冒发烧b.细菌感染c.胃酸过多
(3)材料是人类赖以生存和发展的重要物质基础。
①在下列材料中,属于有机高分子材料的是;属于复合材料的是。
a.硬币b.聚氯乙烯塑料 c.氮化硅陶瓷 d.玻璃钢
②硅酸盐水泥是常用的建筑材料,它主要是以和黏土为原料制成。
③钢铁在潮湿的空气中主要发生的电化学腐蚀是腐蚀,通常用钝化、涂漆、电镀等方法来防止腐蚀。
B.《有机化学基础》
(1)有机化合物的制备、提纯和检验是有机化学研究的基础。
①实验室用乙醇和浓硫酸反应制备乙烯,应将反应温度控制在(填字母。下同)左右。
a.140℃b.170℃c.100℃
②蛋白质提纯可用盐析法,下列盐溶液能用于蛋白质提纯的有。
a.Na2SO4 b.AgNO3c.CuCl2
③鉴别乙酸和甲酸甲酯,可采用的方法是。
a.取样,滴加银氨溶液,水浴加热,观察是否有银镜生成
b.取样,加入乙醇,观察液体是否分层
c.取样,测定试样的核磁共振氢谱,观察谱图中吸收峰的个数
(2)某地近日自来水产生异味,原因是水源被苯酚污染。含苯酚的工业废水必须处理达标后才能排放,苯酚含量在1 g·L-1以上的工业废水应回收苯酚。某研究性学习小组设计下列流程,探究废水中苯酚的回收方法。
①可用为试剂检验水样中是否含有苯酚。
②操作I的名称为,试剂a的化学式为。
③通入CO2发生反应生成苯酚的化学方程式为。
(3)某有机物的分子式为C3H6O3。
①1mol该有机物充分燃烧生成CO2和H2O,消耗O2在标准状况下的体积为L。
②官能团决定有机物的化学性质。取等量的该有机物两份,分别与足量的碳酸氢钠和金属钠反应,生成的气体在同温同压下体积相等。该有机物含有的官能团为、(填名称),请写出该物质的一种结构简式。
③若该有机物两分子间相互反应能生成含有六元环状结构的产物,写出该产物的结构简式。
选考[选修5:有机化学基础]
充分燃烧1.4 g某有机物A生成4.4 gCO2和1.8 g H2O,该有机物蒸气的密度是相同条件下H2密度的28倍。
(1)该有机物的实验式为________,分子式为________。
(2)A的链状同分异构体共________种。
(3)A的链状同分异构体中含有支链的同分异构体的结构简式为________,其名称为________。
(4)B是A的某种同分异构体,B的磁共振氢谱中只有4个信号峰(即只有4种氢原子),B中官能团为_____(用化学式表示),B通入Br2的CCl4溶液褪色,生成化合物C。则由B生成C的化学方程式为________。
选考题[选修3:物质结构与性质]现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大,A元素的价电子构型为nsnnpn+1,C元素为最活泼的非金属元素,D元素核外有三个电子层,最外层电子数是核外电子总数的1/6,E元素正三价离子的3d轨道为半充满状态,F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,G元素与B元素位于同一主族,其外围电子排布是4s24p4,被科学家称为人体微量元素中的“防癌之王”。
(1)A元素的第一电离能________B元素的第一电离能(填“<”“>”或“=”),A、B、C三种元素电负性由小到大的顺序为________(用元素符号表示)。
(2)D元素原子的价电子排布式是________。
(3)C元素的电子排布图为________;E3+的离子符号为________。
(4)F元素符号为________,其基态原子的电子排布式为________。G元素的名称是________。
化工厂的联合生产可以提高资源的利用率,有效减少环境污染,某化工集团将钛的生产和氯碱工业及甲醇生产联合起来,其主要工艺如下: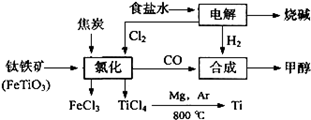
(1)工业电解饱和食盐水的化学方程式为________,其阳极产物为________(填化学式)。
(2)上述工艺流程中钛铁矿在高温条件下经过氯化法得到四氯化钛的化学方程式为________。
(3)已知:① Mg(s) + Cl2(g) = MgCl2(s)△H =" -641" kJ·mol-1
② Ti(s) + 2Cl2(g) = TiCl4(s)△H =" -770" kJ·mol-1
则 2Mg(s) + TiCl4(g) = MgCl2(s) + Ti(s)△H = ________。
(4)在25℃、101kPa条件下,1 g液态甲醇(CH3OH)燃烧生成CO2和液态水时放热22.7 kJ,则表示甲醇燃烧的热化学方程式为:________________________________________。
请根据所学化学知识回答下列问题:
(1)氯化铁溶液蒸干并灼烧后得到的固体物质的化学式是________。
(2)在浓度均为0.1 mol/L的①CH3COONH4②NH4HSO4③NH3.H2O④(NH4)2SO4四种溶液中,NH4+浓度由大到小的顺序为________(用代号表示)。
(3)25时,某浓度的CH3COONa溶液呈碱性的原因是________(用离子方程式表示),溶液中所有离子的浓度由大到小的顺序是________。
(4)某温度下,蒸馏水的pH = 6,氢氧化物R(OH)2的Ksp = 1×10-13,则R2+沉淀完全时,溶液的pH为_______。