硫酸被人们誉为“化学工业之母”,在国民生产中发挥着重要作用,硫酸的产量是衡量一个国家化学工业水平的标志。工业上生产硫酸包括三步:
(1)第一步,在沸腾炉中煅烧黄铁矿,反应如下:4FeS2+11O2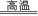 8SO2+2Fe2O3,该反应的氧化产物是 ,当生成8 mol SO2时转移电子的物质的量为 。
8SO2+2Fe2O3,该反应的氧化产物是 ,当生成8 mol SO2时转移电子的物质的量为 。
(2)第二步,在接触室中发生如下反应:2SO2+O2  2SO3。某科技小组的同学在一个恒温恒容的容器中模拟该反应,他们分两次进行实验,第一次向容器中加入2 mol SO2、1 mol O2,反应达平衡后测得SO2的转化率为α1,第二次向容器中加入3 mol SO2、1.5 mol O2, 反应达平衡后测得SO2的转化率为α2,则α1 α2(填“大于”、“等于”或“小于”)。
2SO3。某科技小组的同学在一个恒温恒容的容器中模拟该反应,他们分两次进行实验,第一次向容器中加入2 mol SO2、1 mol O2,反应达平衡后测得SO2的转化率为α1,第二次向容器中加入3 mol SO2、1.5 mol O2, 反应达平衡后测得SO2的转化率为α2,则α1 α2(填“大于”、“等于”或“小于”)。
(3)第三步,在吸收塔中将SO3转化成硫酸。硫酸是化学实验中的常用试剂:
①浓硫酸可以与多种物质发生化学反应,试写出浓硫酸与铜发生反应的化学方程式 。
②有Na、Mg、Al、Cu四种金属,若两两混合后取混合物14 g与足量稀硫酸反应,产生标准状况下H25.6 L,则此混和物的组合方式最多有 种。
某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2—、MnO4—、CO32—、SO42—、SiO32—中的若
干种组成(不考虑水的电离)。取该溶液进行如下实验:
Ⅰ.取适量溶液,加入过量的盐酸,有气体生成,并得到无色溶液;
Ⅱ.在Ⅰ所得溶液中加入过量的NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;
Ⅲ.在Ⅱ所得溶液中加入过量的Ba(OH)2溶液,加热,也有气体生成,同时析出白色沉淀乙。
请回答下列问题:
(1)由实验Ⅰ可知原溶液中一定不含有的离子是________;一定含有的离子是________________。
(2)由实验Ⅱ可知原溶液中还一定含有的离子是________;生成甲的离子方程式为________________。
(3)实验Ⅲ中生成白色沉淀乙的离子方程式为________________。
(4)原溶液中还可能存在的离子是________;检验该离子的方法是_________________。
(1)实验室由纯净的铜屑制胆矾(CuSO4·5H2O)的实验流程如下:
溶解铜屑一种方案是:将铜屑加入到稀硫酸与双氧水的混和液中并用30~40℃水浴加热,一段时间后,铜完全溶解,得到硫酸铜溶液。
①该反应的化学方程式为,
②反应温度不能超过40℃的原因是,
③由硫酸铜溶液获得胆矾的操作依次为、冷却结晶、、洗涤、干燥。
(2)目前我国的火力发电机组绝大多数为燃煤机组,而以燃煤为主的电力生产所造成的环境污染是制约电力工业发展的一个重要因素,其中氮氧化物(NOx)是继粉尘和二氧化硫之后燃煤电站环保治理的重点。
①燃煤烟气脱硫的方法很多,如石灰石—石膏法、氨水法等。其中石灰石-石膏法脱硫的原理第一步是SO2+Ca(OH)2=CaSO3+H2O,然后再将产物氧化制成石膏,写出该反应的化学方程式。
②燃煤烟气脱硝可采用氨(NH3)作为还原介质,在催化剂存在的条件下,氮氧化物(NOx)与还原剂发生反应,生成无害的氮气和水,写出二氧化氮与氨反应的化学方程式。
某校学生化学实验小组,为验证非金属元素氯的氧化性强于硫和氮,设计了一套实验装置(部分夹持装置已略去):
(1)写出A中反应的离子方程式 。
(2)B中出现黄色浑浊现象,产生此现象的离子方程式 。
(3)D中干燥管中出现的现象是,化学方程式 。
(4)有同学认为D中的现象并不能说明氯的氧化性大于氮,需要在C之前加装洗气装置,请指出洗气装置盛装试剂 。
(5)还有什么方法能证明氧化性Cl2>S ,用一种相关事实说明 。
A、B、C、D、F是常见的化合物,其中F在常温下是一种无色液体,D为强酸,请根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
(1)若A、B、C、D均为含硫元素的化合物,A是一种常见的矿石的主要成分,且A的摩尔质量为120 。反应①的化学方程式为;
。反应①的化学方程式为;
(2)若A、B、C、D均为含氮元素的化合物,且A的一个分子中只含有10个电子,则:
①A分子式为__________;
②反应④的离子方程式为________________________________________________
③取Cu和Cu2O的混合物样品12.0g,加入到足量的D的稀溶液中,用排水法收集产生的气体,标准状况下其体积为2.24L,则样品中Cu2O的质量为__________g。
(1)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。甲、乙两元素相比较,金属性较强的是(填名称),
可以验证该结论的实验是。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
(2)通常情况下,微粒X和Y为分子,Z和W为阳离子,E为阴离子,它们都含有10个电子;
Y溶于X后所得的物质可电离出Z和E;X、Y、W三种微粒反应后可得Z和一种白色沉淀。请回答:
①用化学符号表示下列4种微粒:X:Y :Z:E :
②写出两个X、Y、W三种微粒反应的离子方程式:、