(共10分)
有一类烷烃,其分子中只有一种氢原子(即:一卤代物只有一种的烷烃)。此系列烷烃的第二项可看成CH4及C2H6分子中所有氢原子被甲基(CH3-)代替后所得。CH4分子的空间形状可看成球形,而C2H6分子的空间形状可看成椭球形
(1)下表为一卤代物都只有一种的球形烷烃及椭球形烷烃系列,填写下表空白处。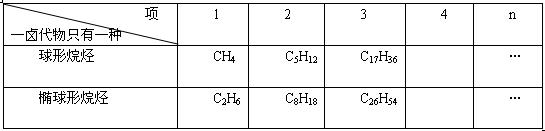
(2)只有一种氢原子的球形烷烃或椭球形烷烃系列中,相邻的两项中,后者每个分子中氢原子数是前者每个分子中氢原子数的 倍
(3)根据上表中“一卤代物只有一种的烷烃”的分子式中有关规律,请你分别写出这两类烷烃的通式(通式中要求当n=1时,上述两系列的第一项分别为CH4及C2H6)。
①一卤代物只有一种的球形烷烃的通式是 。
②一卤代物只有一种的椭球形烷烃的通式是 。
图示法和图像法都是常用的科学研究方法。
(1)科学家通过X射线推测胆矾中既含有配位键又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示。
①写出基态Cu原子的核外电子排布式________________________________。
②写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)________。
(2)下图是研究部分元素氢化物的沸点变化规律的图像,折线c可以表达出第________族元素氢化物的沸点变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线——折线a和折线b,你认为正确的是________(填“a”或“b”),理由是______________________________________________________________。
(3)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫做第一电离能(设为E)。如图所示:
①同周期内,随着原子序数的增大,E值变化的总趋势是________;
②根据图中提供的信息,试推断E氧________E氟(填“>”、“<”或“=”,下同);
③根据第一电离能的含义和元素周期律,试推断E镁________E钙。
现有5种固态物质:氯化钠、硼、石墨、锑、氖。将符合信息的物质名称和所属晶体类型填在表格中。
| 编号 |
信 息 |
物质名称 |
晶体类型 |
| (1) |
熔点811 ℃,硬度较大,易溶于水,水溶液或熔融态时均能导电 |
||
| (2) |
熔点630.74 ℃,沸点1 750 ℃,导电 |
||
| (3) |
由分子间作用力结合而成,熔点很低,化学性质稳定 |
||
| (4) |
由共价键结合成空间网状结构的晶体,熔点2 300 ℃,沸点2 550 ℃,硬度大 |
||
| (5) |
由共价键结合成层状结构的晶体,熔点高、能导电,具有滑腻感 |
你注意到汽车加油站内的标牌了吗?某些省市加油站提供的汽油标号由90#、93#换成了E90、E93,后者是在汽油中加入了10%的燃料乙醇而制得的乙醇汽油。燃料乙醇的生产过程可由下图表示:
(1)粉碎玉米的目的是_______________________________________________。
(2)生产过程中为了检验淀粉水解是否完全,可使用的试剂是________。
(3)步骤a的操作是________(填字母)。
| A.蒸发 | B.萃取 | C.蒸馏 | D.分液 |
(4)发酵产生的CO2纯度可达到99%,能回收利用,请举出它的两项用途:________、________。
(5)以玉米淀粉为原料生产乙醇的化学反应可用下式表示:
(C6H10O5)n+nH2O nC6H12O6
nC6H12O6
C6H12O6―→2C2H5OH+2CO2↑
根据上述反应式,可以算出100 kg淀粉理论上可生产无水乙醇________ kg。
实验室制备甲酸铜晶体[Cu(HCOO)2·4H2O]的流程如下:
回答下列问题:
(1)小苏打水溶液显________性(填“酸”、“碱”或“中”)可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为________________________。
(2)生成碱式碳酸铜[Cu2(OH)2CO3]的离子方程式为________________________。
(3)操作a的名称是________,该操作使用的玻璃仪器有________。
(4)证明碱式碳酸铜已经洗涤充分的实验操作是________________________________。
(5)用无水乙醇洗涤晶体的目的是___________________________________。
A、B、C、X均为中学常见的纯净物,它们之间有如图转化关系(副产物已略去)。
回答下列问题:
(1)若X是强氧化性单质,则A不可能是________。
a.S b.N2 c.Na d.Mg e.Al
(2)若A、B、C为含金属元素的无机化合物,X为强电解质溶液,A溶液与C溶液反应生成B,则B的化学式为________,X的化学式可能为(写出不同类物质)________或________,反应①的离子方程式为________________________或________________________。