已知化合物甲和乙都不溶于水,甲可溶于质量分数大于或等于98%的硫酸,而乙不溶。现有一份甲和乙的混合物样品,通过实验进行分离,可得到固体甲。(实验中使用的过滤器是用于过滤强酸性液体的耐酸过滤器)
请填写表中空格,完成由上述混合物得到固体甲的实验设计。
(1)某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。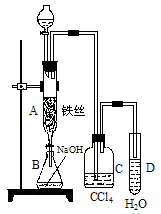
①写出A中有机反应的化学方程式 。
②已知上述有机反应是放热反应,观察到A中的现象是:
及_____ _________。
③ 实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关的化学方程式 。
④C中盛放CCl4的作用是 。
⑤能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中滴入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入______ _____,现象是______________________。
(2)乙炔的实验室制法
①反应原理_____ ____________。
②选择合适的制取实验装置___ ___。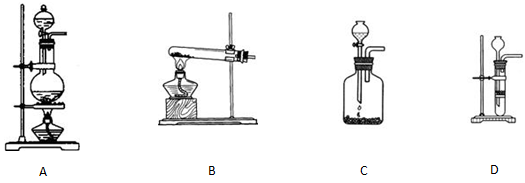
③实验中常用饱和食盐水代替水,目的是______ __________。
④纯净的乙炔气体是无色无味的气体,用电石和水反应制取的乙炔,常含有H2S和PH3而有恶臭气味。可以用____ _______溶液除去杂质气体。
.选择适当的试剂和方法除去下列物质中所含的少量杂质(括号内为杂质):
| 物质 |
试剂 |
方法 |
| (1)乙烷(乙烯) |
||
| (2)溴苯(溴) |
||
| (3)乙醇(水) |
||
| (4)乙酸乙酯(乙酸) |
||
| (5)苯甲酸(NaCl) |
影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。实验药品:铜、铁、镁、0.5mol/LH2SO4、2mol/LH2SO4、、18.4mol/LH2SO4
A:甲同学研究的实验报告如下表:
| 实验步骤 |
现象 |
结论 |
| ①分别取等体积的2mol/L的硫酸于试管中 ② |
反应速率镁>铁,铜不反应 |
金属的性质越活泼,反应速率越快 |
(1)甲同学表中实验步骤②为。
(2)甲同学的实验目的是;要得出正确的实验结论,还需控制的实验条件是。B:乙同学为了更精确的研究浓度对反应速率的影响,利用下图所示装置进行实验
(3)乙同学在实验中应该测定的数据是。
(4)乙同学完成该实验应选用的实验药品。该实验中不选用某浓度的硫酸,理由是。
用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.20mol·L -1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
| NaOH起始读数 |
NaOH终点读数 |
|
| 第一次 |
0.10mL |
18.60mL |
| 第二次 |
0.30mL |
18.00mL |
(1)根据以上数据可以计算出盐酸的物质的量浓度为mol·L-1.
(2)达到滴定终点的标志是
某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度完成以下填空:
(1)正确操作的顺序是(用序号字母填写)______________________.
(2)上述(B)操作不用标准溶液润洗滴定管,则对测定结果的影响是(填偏大、偏小、不变,下同)_____________。
(3)滴定结束后如仰视观察滴定管中液面刻度,则对滴定结果的影响是___________。