工业“从海水中提取镁”的流程图如下:
其步骤为:
①将海边大量存在的贝壳煅烧成石灰,并将石灰制成石灰乳;
②将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;
③在Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl2·6H2O;
④将MgCl2·6H2O在一定条件下加热得到无水MgCl2;
⑤电解熔融的氯化镁可得到Mg。
请回答以下问题:
⑴步骤③中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有 、 、酒精灯、铁架台等。
⑵步骤④中的“一定条件”指的是 ,目的是 。
⑶上述提取镁的流程中,在降低成本、减少污染方面做了一些工作,请写出其中一点:
。
⑷有同学认为:步骤②后可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则。你同意该同学的想法吗?为什么?
你的观点是 。理由是
。
(1)A、B、C、D为四种短周期主族元素,且原子序数依次增大。已知A的最外层电子数是其电子层数的2倍,B是地壳中含量最高的元素,B原子的最外层电子数是D原子最外层电子数的2倍,C原子最外层只有一个电子。则元素符号为A,
B,C,D;D的最高价氧化物对应水化物的化学式为;AB2 的电子式为。
(2)海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验,请回答有关问题。
(ⅰ)步骤①灼烧海带时,除需要三脚架、坩埚、泥三角外,还需要用到下列仪器中的。
A.烧杯 B. 酒精灯 C.表面皿 D. 干燥器
(ⅱ)步骤③的实验操作名称是;步骤⑥的目的是从含碘苯溶液中分
离出单质碘和回收苯,该步骤的实验操作名称是。
(ⅲ)步骤④的反应中碘离子被(填“氧化”或“还原”)。
(ⅳ)检验单质碘的方法是。
动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
| 实验步骤 |
实验现象 |
||||
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
|
||||
| ⑤将铝条投入稀盐酸中 |
E.生成白色胶状沉淀,继而沉淀消失 |
||||
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉锭。 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究 性质递变规律。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等。
仪器:① ,② ,烧杯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号)(各1分)
| 实验内容 |
① |
② |
③ |
④ |
⑤ |
⑥ |
| 实验现象(填A~F) |
步骤①的化学方程式: ,
步骤⑥的离子方程式 ,
此实验的结论: 。
现有短周期元素X形成的单质A与NaOH溶液反应,有如下转化关系(若产物中有水生成则省略未表示出来): 。
。
(1)若常温常压下,A为气态,且B、C中均有X元素,则A与NaOH溶液反应的离子方程式为,实验室制备A的化学方程式为;
(2)若常温常压下,A为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为;
(3)若A为金属,C为气体,则A 与NaOH溶液反应的离子方程式为
;其最高氧化物与NaOH溶液反应的离子方程式为;
(4)由(2)和(3)中两种单质形成合金在工业、建筑业中有重要的用途。一个探究性学习小组,他们拟用该合金与足量稀硫酸的反应测定通常状况下气体摩尔体积,实验装置如下: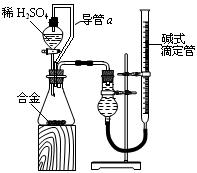
①装置中导管a的作用是;
②实验中准确测得4个数据:实验前该合金的质量m1 g,实验后残留固体的质量m2 g,实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL;则通常状况时气体摩尔体积Vm=____________L·moL-1。
如图是实验室制取酚醛树脂的装置图(烧杯底部垫有石 棉网)。
棉网)。
(1)装置中的一处错误是______________________________
(2)试管上方长玻璃管的作用是_______________________________
(3)浓盐酸在该反应中的作用是_______________________________
(4)实验完毕后,若试管用水不易洗涤,可以加入少量_______浸泡几分钟,然后洗净。
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品 。
。
请回答下列问题:
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入_________________________________。
(2)反应中加入过量的乙醇,目的是__________________________________________________。
(3)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图: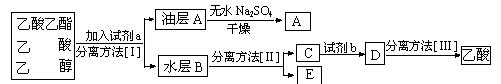
则试剂a是:______,分离方法I是______,分离方法II是______,
试剂b是________,分离方法III是_____________ _。
_。