(1)冶炼金属常用以下几种方法:①还原法,②电解法,③热分解法。下列金属各采用哪种方法还原最佳。(用序号填写下列空白。)
Ⅰ.Fe、Zn、Cu 等中等活泼金属 。
等中等活泼金属 。
Ⅱ.Na 、Mg、Al等活泼或较活泼金属 。
、Mg、Al等活泼或较活泼金属 。
Ⅲ.Hg、Ag等不活泼金属 。
(2)写出以锌片、铜片为两极,稀硫酸溶液为电解质溶液组成的原电池的电极反应式:
负极: ;正极: 。
一定温度下的密闭容器中存在如下反应:
CO(g)+H2O(g) CO2(g)+ H2(g),已知CO(g)和H2O(g)的起始浓度均为2 mol·L-1,经测定该反应在该温度下的平衡常数K =1,试判断:
CO2(g)+ H2(g),已知CO(g)和H2O(g)的起始浓度均为2 mol·L-1,经测定该反应在该温度下的平衡常数K =1,试判断:
(1)当CO转化率为25%时,该反应是否达到平衡_______,若未达到平衡,向哪个方向进行______。
(2)达到平衡时,CO的转化率____________________。
(3)当CO的起始浓度仍为2 mol·L-1,H2O(g)的起始浓度为6 mol·L-1,求平衡时CO的转化率_______。
在一定条件下,可逆反应A2(g)+B2(g) 2C(g)在一个密闭容器中达到平衡时,测得c(A2)=0.5mol·L-1,c(B2)=0.1mol·L-1,c(C)=1.6mol·L-1。若
2C(g)在一个密闭容器中达到平衡时,测得c(A2)=0.5mol·L-1,c(B2)=0.1mol·L-1,c(C)=1.6mol·L-1。若 、
、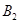 、C的起始浓度分别为a mol·L-1、b mol·L-1、g mol·L-1请确定:
、C的起始浓度分别为a mol·L-1、b mol·L-1、g mol·L-1请确定:
(l)a、g应满足的关系式为_____________。
(2)若反应从正反应方向开始进行,当g=_________,a有最大值为__________。
(3)若反应从逆反应方向开始进行,当b=_________,a有最小值为_________.
(4)b的取值范围为___________________。
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚( CH3OCH3)。请回答下列问题:
(1)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)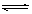 CH3OH(g)△H= -90.8kJ/mol
CH3OH(g)△H= -90.8kJ/mol
②2CH3OH(g)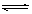 CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
③CO(g)+H2O(g)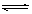 CO2(g)+H2(g)△H=-41.3kJ/mol
CO2(g)+H2(g)△H=-41.3kJ/mol
总反应:3H2(g)+3CO(g)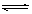 CH3OCH3(g)+CO2(g) 的△H= ;
CH3OCH3(g)+CO2(g) 的△H= ;
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是:
________(填字母代号)。
a.压缩体积 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度
e.分离出二甲醚(CH3OCH3)
(2)已知反应②2CH3OH(g)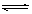 CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| 浓度(mol·L-1) |
0.40 |
0.6 |
0.6 |
①比较此时正、逆反应速率的大小比较: _________
_________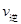 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②该反应的平衡常数的表达式为K=_____,温度升高,该反应的平衡常数K____(填“增大”、“减小”或“不变”)
工业上利用CO和水蒸气在一定条件下发生反应制取氢气:CO(g)+H2O(g) CO2(g)+H2(g)某研究小组分别在体积均为2L的恒容密闭容器中加入一定量的反应物,使其发生反应,相关数据如下:
CO2(g)+H2(g)某研究小组分别在体积均为2L的恒容密闭容器中加入一定量的反应物,使其发生反应,相关数据如下:
| 容器编号 |
温度℃ |
起始量/mol |
平衡量/mol |
达到平衡的时间/min |
达到平衡时体系能量的变化/kJ |
||
| CO |
H2O |
CO2 |
H2 |
||||
| ① |
650 |
1 |
2 |
0.4 |
0.4 |
5 |
16.4 |
| ② |
650 |
2 |
4 |
t1 |
Q1 |
||
| ③ |
900 |
2 |
4 |
1.6 |
1.6 |
t2 |
Q2 |
(1)计算容器②中反应的平衡常数K=_____________(计算结果保留两位小数)。
(2)容器③中反应达平衡时,CO的转化率为____________。
(3)容器①中反应达平衡这段时间,化学反应速率 =__________。
=__________。
(4)该反应的正反应为_______(填“吸热”或“放热”)反应,理由是____________。
(5)下列叙述正确的是____________(填字母序号)。
a.平衡时,容器①和容器②中CO2的体积分数相等
b.反应达平衡状态时,Q2>Q1>32.8kJ
c.达到平衡的时间:t2>t1>2.5min
d.该反应的热化学方程式可表示为:CO(g)+H2O(g) CO2(g)+H2(g)△H= -41kJ/mol
CO2(g)+H2(g)△H= -41kJ/mol
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察右图,然后回答问题。
(l)图中所示反应是______(填“吸热”或“放热”)反应,该反应_______(填“需要”或“不需要”)加热,该反应的△H=_______(用含 、
、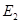 的代数式表示)。
的代数式表示)。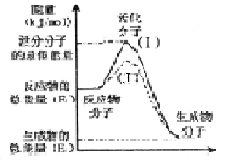
(2)已知热化学方程式:H2(g) +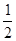 O2(g)═H2O(g);△H=-241.5kJ/mol,该反应的活化能为167. 4kJ/mol,则其逆反应的活化能为________________。
O2(g)═H2O(g);△H=-241.5kJ/mol,该反应的活化能为167. 4kJ/mol,则其逆反应的活化能为________________。
(3)对于同一反应,图中虚线(Ⅱ)与实线(I)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是_____________。