元素推断题:
X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)M的元素符号为 ;X、Y、Z、L四种元素的原子半径从大到小的顺序是 (用元素符号表示)。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为 ,B的结构式为____________。
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______,其最高价氧化物对应的水化物化学式为 。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。
a.+99.7 kJ·mol-1 b.+29.7 kJ·mol-1 c.-20.6 kJ·mol-1 d.-241.8 kJ·mol-1
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如下图所示,请回答:
(1)“O”点导电能力为0的理由是 。
(2)A、B、C三点溶液c(H+)由小到大的顺序为 。
(3)若使C点溶液中c(CH3COO-)增大的同时溶液的c(H+)减小,可采取的措施是:
① ;② ;③ 。
(4)经实验测得C点处:c(CH3COOH)="0.1" mol·L-1,c(CH3COO-)="0.01" mol·L-1,则该条件下CH3COOH的电离常数Ka= 。
(1)下列物质:①石墨 ②三氧化硫 ③液态氯化氢 ④氯气 ⑤熔融的硫酸钾 ⑥食盐晶体 ⑦硫酸溶液 ⑧乙醇 ⑨冰醋酸 ⑩NH3·H2O,其中能够导电的是 ,强电解质是 ,弱电解质是 ,非电解质是 。
(2)H2S溶于水的电离方程式为 。
①向H2S溶液中加入CuSO4溶液时,电离平衡向 移动,c(H+) ,c(S2-) 。
②向H2S溶液中加入NaOH固体时,电离平衡向 移动,c(H+) ,c(S2-) 。
③若将H2S溶液加热至沸腾,c(H2S) 。
④若要增大H2S溶液中c(S2-),最好加入 。
有A、B、C、D四个反应:
| 反应 |
A |
B |
C |
D |
| ΔH/(kJ·mol-1) |
10.5 |
1.80 |
-126 |
-11.7 |
| ΔS/(J·mol-1·K-1) |
30.0 |
-113.0 |
84.0 |
-105.0 |
则在任何温度下都能自发进行的反应是 ;任何温度下都不能自发进行的反应是 ;另两个反应中,在温度高于 ℃时可自发进行的反应是 ;在温度低于 ℃时可自发进行的反应是 。
氨的工业合成工艺的成熟推动了人类文明的进步,不少科技工作者为了寻找廉价的氨的制备方法,进行了前赴后继的探索性工作。请回答下列各题:
用氢气和氮气合成氨是一个可逆反应,化学方程式如下:N2+3H2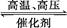 2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
(1)请写出该反应的热化学方程式 。
(2)如果一个反应的ΔH-TΔS<0,则该反应能够自发进行。已知该反应的ΔS="-198.2" J·K-1·mol-1。则上述氨气的合成反应在常温下 (填“能”或“不能”)自发进行。
(1)科学家根据体系存在着力图使自身能量趋于 和由 变为 的自然现象,提出了互相关联的 判据和 判据,为最终解决“反应进行的方向”这一问题提供了必要的依据。
(2)在密闭条件下,体系有有序自发地转变为无序的倾向,因为与有序体系相比,无序体系更加稳定,科学家把这种因素称作 。
(3)判断下列过程熵变的正负(填“>0”或“<0”):
①溶解少量蔗糖于水中,ΔS ;
②纯碳和氧气反应生成CO(g),ΔS ;
③液态水蒸发变成水蒸气,ΔS ;
④CaCO3(s)加热分解生成CaO(s)和CO2(g),ΔS 。