氨的工业合成工艺的成熟推动了人类文明的进步,不少科技工作者为了寻找廉价的氨的制备方法,进行了前赴后继的探索性工作。请回答下列各题:
用氢气和氮气合成氨是一个可逆反应,化学方程式如下:N2+3H2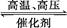 2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
(1)请写出该反应的热化学方程式 。
(2)如果一个反应的ΔH-TΔS<0,则该反应能够自发进行。已知该反应的ΔS="-198.2" J·K-1·mol-1。则上述氨气的合成反应在常温下 (填“能”或“不能”)自发进行。
(8分)下列有机物中,有多个官能团: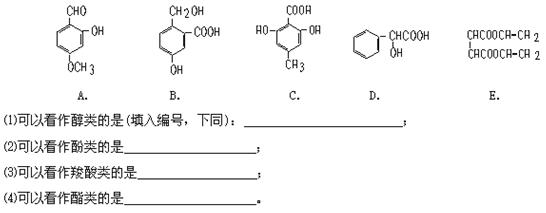
有机物A 0.02 mol 在氧气中完全燃烧生成4.4g CO2和2.16g H2O,无其它物质生成。试回答下列问题:
⑴下列说法中正确的是(填写序号)
| A.该化合物肯定含O元素 | B.该化合物可能不含O元素 |
| C.该化合物肯定不能和Na反应 | D.该分子中C:H的个数比为5:12 |
⑵若A为烃,且它的一卤代物只有一种结构,此烃的结构简式为:。用系统法命名为:。此烃共有种同分异构体。
⑶若A为一元醇且在空气中不能被Cu催化氧化成相应的醛。则A的结构简式为,其名称(系统命名)为
1mol醇A与足量钠反应,可生成H2的体积为L(STP).
为了减少温室气体排放,目前工业上采用CO2与H2在CuO-ZnO/ZrO催化下反应制备重要化工原料CH3OH的工艺:CO2(g)+3H2(g)  CH3OH(g)+H2O(g);⊿H<0。为了探究其反应原理进行如下实验,在2L密闭容器内250℃条件下,测得n(CO2)随时间的变化情况如下表:
CH3OH(g)+H2O(g);⊿H<0。为了探究其反应原理进行如下实验,在2L密闭容器内250℃条件下,测得n(CO2)随时间的变化情况如下表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| n(CO2)(mol) |
0.40 |
0.35 |
0.31 |
0.3 |
0.3 |
0.3 |
根据题目回答下列问题:
(1)0~3 s内用H2表示的平均反应速率是,
(2)平衡时CO2的转化率是。
(3)能说明反应已达平衡状态的是。
A.υ(H2)=3υ(CO2) B.容器内压强保持不变
C.υ逆(CO2)=υ正(CH3OH) D.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是。(填序号)
A.及时分离出产物 B.适当升高温度
C.增大CO2浓度 D.选择适当的催化剂
(6分) 铅蓄电池是最普通的二次电源,其电极材料分别是Pb和PbO2,电解质溶液为稀硫酸。工作时,该电池的总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O。已知PbSO4是难溶性的电解质,根据上述情况判断:
(1)蓄电池的负极是,其电极反应方程式为。
(2)蓄电池的正极反应方程式为:PbO2 + 2e- + 4H+ +SO42- = PbSO4 + 2H2O,当电路中转移3mol电子时,被还原的PbO2的物质的量为。
(3)蓄电池工作时,其中电解质溶液的pH______(填“增大”、“减小”、“不变”)。
某人设计的糖厂甘蔗渣利用方案如下图所示:
其中:A能催熟水果,B是高分子化合物,D是有水果香味的物质。
请回答以下问题:
(1)“C6H12O6”所示的物质的名称是_________,A的电子式为_______________。
(2)写出下列转化的化学方程式并指出反应类型:
A→B ___________________________________,反应类型__________________。
C→D____________________________________,反应类型__________________。
CH3CH2OH→CH3CHO:___________________________________,反应类型__________________。