下列离子方 程式中正确的是
程式中正确的是
| A.锌片插入硝酸银溶液中:Zn+Ag+ = Zn2++Ag |
| B.往碳酸钙中滴加稀盐酸:CO32-+2H+=CO2↑+H2O |
| C.氢氧化钡溶液和稀硫酸反应: Ba2++ SO42-= BaSO4↓ |
| D.氢氧化钠溶液中加入过量碳酸氢钙溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
下列各选项所述的两个量,前者一定大于后者的是
①Al原子和N原子的未成对电子数②Ag+、Cu2+与NH3形成配合物时的配位数
③NaCl的晶格能与MgO的晶格能④F元素和O元素的电负性
⑤N元素和O元素的第一电离能⑥H原子和H+离子的半径
| A.①④⑤ | B.②④⑥ | C.④⑤⑥ | D.③⑤⑥ |
2008年震惊我国的“毒奶粉”事件,是奶粉中掺有一种叫三聚氰胺的物质(分子结构如图),其分子式为C3N6H6,是一种白色无味的晶体。下列有关三聚氰胺的说法不正确的是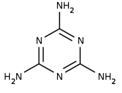
| A.它是一种含氮的有机化合物,所有碳原子都采用sp2杂化 |
| B.它的相对分子质量为126 g/mol |
| C.它易溶于苯、四氯化碳等有机溶剂 |
| D.由于它的含氮量高,被不法商人添加到奶粉中,以提升奶粉检测中的蛋白质含量指标 |
下列各组说法均不正确的是
① CH3—CH=CH2和CH2=CH2的最简式相同② CH≡CH和C6H6含碳量相同
③正戊烷、异戊烷、新戊烷的沸点逐渐变低④丁二烯和丁烯为同系物
⑤标准状况下,11.2 L的戊烷所含的分子数为0.5 NA(NA为阿伏加德罗常数)
⑥能够快速、微量、精确的测定相对分子质量的物理方法是核磁共振氢谱法
| A.①②⑥ | B.②③④ | C.②③⑥ | D.④⑤⑥ |
历史上最早应用的还原性染料是靛蓝。春秋时期,我国先民已能从蓝草中提出这种染料,早于欧洲1500多年。其结构简式如图所示:下列关于靛蓝的叙述,错误的是
| A.靛蓝由碳、氢、氧、氮4种元素组成 |
| B.它的分子式是C16H10N2O2 |
| C.该物质是高分子化合物 |
| D.它是不饱和的有机物 |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
| A.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 |
| B.NH3分子中N原子形成三个杂化轨道,CH4中C原子形成4个杂化轨道 |
| C.两种中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 |
| D.以上说法都不正确 |