用18mol/L 浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④转移、洗涤 ⑤定容、摇匀
回答下列问题
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是
(从下列中选用 A. 10ml B. 25ml C. 50ml D. 100ml)
(2)第③步实验的操作是
(3)第⑤步实验的操作是
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视溶液的液凹面
(Ⅰ)A、B、C和D代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①C的原子序数是A、B的原子序数之和,A、C、D的最外层电子数和为13;
②D的原子序数是C的2倍,D的最高价氧化物对应的水化物是二元强酸。
试根据以上叙述回答:
(1)B单质的电子式为,画出C元素的原子结构示意图;
(2)下列环境问题与B与C形成的化合物有关的是;
A.温室效应 B.光化学烟雾 C.酸雨 D.PM2.5
(3)A、B、C和D四种元素可形成一化合物,其原子个数之比为8∶2∶4∶1。该化合物属于(填晶体类型)。
(Ⅱ)现有下列短周期元素相关性质的数据:
| 元素编号 元素性质 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
| 原子半径(10-10m) |
0.74 |
1.60 |
1.52 |
1.10 |
0.99 |
1.86 |
0.75 |
| 最高正化合价 |
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
|
| 最低负化合价 |
-2 |
-3 |
-1 |
-3 |
试回答下列问题:
(1)元素⑤在周期表中的位置;元素②的单质与CO2反应的化学方程式,该单质可通过电解法制得,下列金属中人类最早开发和利用的是;
A.铁 B.铝 C.金 D.铜
(2)元素④与元素⑦相比较,气态氢化物较稳定的是(填结构式);
(3)元素④形成的+3和+5价的氯化物中,各原子均达到8电子稳定结构的化合物是。(写化学式)
下图每一个字母代表一种反应物或生成物。已知在常温下A是固体,B、C、E、F、G均为气态化合物,其中B、E为气态氢化物,X为空气中的常见成分之一。根据下列反应框图填空(有些反应条件已略去)。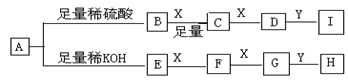
(1)工业上C→D的设备名称是;
(2)当小心加热H与E化合生成的物质时,分解得到一种与CO2具有相同原子数目和相同电子数目的气体,同时还有一种无色无味的液体生成。试写出相应的化学方程式
__________;
(3)I的浓溶液有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是;
A.酸性 B.脱水性 C.强氧化性 D.吸水性
(4)在铁和铜的混合物中,加入一定量的H的稀溶液,充分反应后剩余m1 g金属,再向其中加入一定量的I的稀溶液,充分振荡后,剩余m2 g金属,则m1 与m2之间的关系是。
A.m1一定大于m2 B.m1 可能等于m2
C.m1一定等于m2 D.m1 可能大于m2
某有机物A由C、H、O三种元素组成,现取21.6g A在足量氧气中完全燃烧,将燃烧产物全部依次通过无水氯化钙和碱石灰后,固体质量的增加依次为14.4g和61.6g。用质谱法分析得知A的相对分子质量为108。试回答:
(1)A的分子式是。
(2)经红外光谱测定,A分子结构中含有苯环和羟基;则A所有可能的结构简式是
。
(3)若A能与烧碱反应,且苯环上有二种环境的氢,则A与氢氧化钠反应的化学方程式是。
以苯酚为原料合成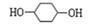 的路线如下所示,请按要求作答:
的路线如下所示,请按要求作答:
(其中E的结构简式为: )
)
(1)物质A的分子式为;写出鉴别苯酚与物质A所需的试剂是。
(2)反应②的反应条件是。物质D的官能团名称是。
(3)写出以下物质的结构简式:
B,F。
(4)写出反应③、④的化学反应方程式:
③;
④。
R、X、Y、Z、Q、W是六种原子序数依次增大的短周期元素,其相关信息如下表:
| 元素 |
相关信息 |
| R |
R在周期表中的周期数、族序数与其原子序数均相等 |
| X |
X原子形成的化合物种类最多 |
| Y |
Y的氢化物与其最高价氧化物的水化物化合生成一种盐 |
| Z |
Z原子的最外层电子数为K层电子数的3倍 |
| Q |
Q存在质量数为23,中子数为12的核素 |
| W |
W在所处周期中原子半径最小 |
(1)Y的元素名称,它在元素周期表中位置是;
(2)元素非金属性X比W (填“强”或“弱”); X和W的最高价氧化物对应的水化物中,酸性较强的是(写化学式)
(3)R与X形成的化合物中,分子中R、X原子个数比为1:1,且分子中只有一种环境的R原子,常温下呈液态,该物质的结构简式是。R、X、Z可以形成X2R6Z2化合物,1mol该物质与足量的金属钠反应生成1mol氢气,则该物质的结构简式是,请写出该物质的一种主要用途。