实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验。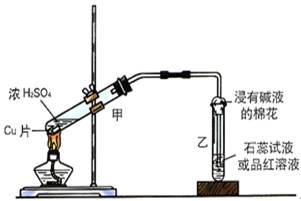
(1)根据什么现象可判断铜跟浓硫酸反应有SO2生成___________ _____。
根据什么现象可判断铜跟浓硫酸反应有硫酸铜生成___________ _________。
写出甲装置中发生的主要反应的化学方程式________________________
(2)你在实验室中进行这个实验时,除了(1)小题中指到的实验现象外,还可以观察到许多其它的实验现象,请写出两种:____________________________________________________。
(3)装置乙的试管口部放有一团浸有碱液的棉花,棉花中通常是浸有饱和碳酸钠溶液,写出棉花中发生反应的化学方程式 。
下图为制取乙酸乙酯的实验装置图。回答下列问题: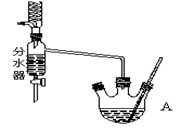
揭示实验原理
①乙酸与乙醇在催化剂存在的条件下加热可以发生反应生成乙酸乙酯。请用氧同位素示踪法写出乙酸与乙醇发生酯化反应的化学方程式______________________。
②能否用氢同位素示踪法揭示酯化反应原理?_______(选填“能”或“否”),原因是___________。
反应温度确定:
合成乙酸乙酯的反应为放热反应。实验表明,反应温度应控制在85℃左右为宜。回答:
实验温度不宜低于85℃左右的原因是__________________________________________;
实验温度不宜高于85℃左右的原因是__________________________________________;
实验装置的比较:
利用上图装置制备乙酸乙酯,这种装置与教材装置相比较突出的优点是___________。
酯层厚度的标示:
为更好地测定酯层厚度,可预先向饱和Na2CO3溶液中滴加1滴____试液,现象是___________。
下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
[实验目的]制取乙酸乙酯
[实验原理]甲、乙、丙三位同学均采取乙醇(CH3CH218OH)、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,其中浓硫酸除了作吸水剂的作用外还有
[装置设计]甲、乙、丙三位同学分别设计了下列三套实验装置:
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,我选择的装置是 (选填“甲”或“乙”)。丙同学将甲装置中的玻璃管改成了球形干燥管除起冷凝作用外,它的另一重要作用
是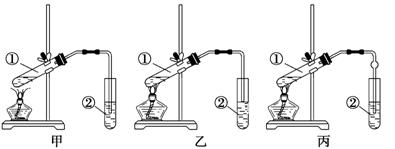
[实验步骤]
(1)按选择的装置组装仪器,在试管中先加入3mLCH3CH218OH,2mL冰醋酸,并在摇动下缓缓加入2mL浓硫酸充分摇匀,
(2)将试管固定在铁架上;
(3)在试管②中加人适量的饱和Na2CO3溶液;
(4)用酒精灯对试管①加热;
(5)当观察到试管②中有明显现象时停止实验。
[问题讨论]
a.根据试管②中观察到的现象,可知乙酸乙酯的物理性质有:
无色油状液体、 ;
b.试管②中饱和Na2CO3的作用是溶解乙醇、降低乙酸乙酯的溶解度还有 的作用,从试管②中分离出乙酸乙酯的实验操作是 ,生成乙酸乙酯的化学反应方程式
实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表。
| 化合物 |
相对分子质量 |
密度/g·cm-3 |
沸点/℃ |
溶解度/100g水 |
| 正丁醇 |
74 |
0.80 |
118.0 |
9 |
| 冰醋酸 |
60 |
1.045 |
118.1 |
互溶 |
| 乙酸正丁酯 |
116 |
0.882 |
126.1 |
0.7 |
请回答有关问题。
Ⅰ.乙酸正丁酯粗产品的制备
在A中加入11.5mL正丁醇和7.2mL冰醋酸,再加3~4滴浓硫酸,混合均匀,投入沸石。如图所示安装分水器、温度计及回流冷凝管,并在分水器中预先加水至略低于支管口,加热回流,反应一段时间将水逐渐分去,至反应完毕。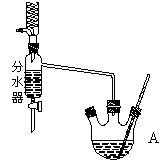
(1)仪器A中发生反应的化学方程式为____________________________。有同学拟通过某种方法鉴定所得产物中是否含有杂质,可采用 确定。
a.红外光谱法 b.1H核磁共振谱法c.质谱法
(2)“反应中利用分水器将水分去”该操作的目的是: 。
(3)反应时加热有利于提高酯的产率,但温度过高酯的产率反而降低,其可能的原因是 。
(4)可根据 现象来判断反应完毕。
Ⅱ.乙酸正丁酯粗产品的精制
(5)将仪器A中的液体转入分液漏斗中,用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是 。
(6)再用10ml 10% Na2CO3溶液洗涤有机层,该步操作的目的是 。
(7)将干燥后的产品蒸馏收集乙酸正丁酯产品时,应将温度控制在 左右。
请你与某小组的同学共同探究乙醇与乙酸的酯化反应实验: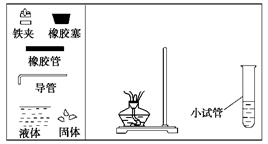
(1)请你根据图示,补画实验室制取乙酸乙酯的装置图。
(2)其中小试管中装入的物质是____________;其主要作用是 、 __________、__________________________。
(3)分离小试管中制取的乙酸乙酯应使用的仪器叫做_________;分离完毕,应从该仪器_______(填“下口放”或“上口倒”)出。
(4)实验完毕,发现大试管中的反应液有些变黑,其原因是________________________。
(5)该实验中,若用3mol乙醇和1mol乙酸在浓硫酸作用下加热,充分反应后,能否生成1mol乙酸乙酯? (填“能”或“不能”),原因是 (不考虑原料损耗)。
(6)写出该反应的化学方程式:
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常用冰醋酸、无水乙醇和浓硫酸混合,在加热条件下反应制得:
请根据要求回答下列问题:
(1)c写出该反应的化学方程式
(2)此反应中浓硫酸的作用是
饱和碳酸钠的作用是
(3)若采用同位素示踪法研究该化学反应,反应物无水乙醇中含有18O,冰醋酸中均为16O,反应后的混合物中,含有18O的物质有
(4)若用如图所示装置来制备少量的乙酸乙酯,锥形瓶中的现象为 ,不过往往产率偏低,其原因可能为 (任填2种)