X、Y、Z、W、R是五种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y 元素原子的最外层电子数是其次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。请填写下列空白:
(1)画出W的原子结构示意图; 。
(2)Z和W最高价氧化物的水化物的碱性较强的是: (写化学式),它们之间在溶液中反应的离子方程式是; ;
(3)Z2Y2 中阴离子的化学式是 。
(4)在同周期元素中,R 元素及与其相邻元素的原子半径从大到小的顺序是: 。与R元素同周期且非金属性最强的元素是: 。
(5)W的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料,其反应的化学方程式是: 。
(14分)某课外活动兴趣小组欲用下列化学试剂在实验室里制取Cl2并验证Cl2的某些化学性质。实验试剂:3 mol·L-1 H2SO4、1 mol·L-1 NaOH溶液、MnO2、KMnO4、吸收少量SO2的NaOH溶液、浓盐酸、紫色石蕊试液、饱和NaCl溶液、BaCl2溶液、品红溶液。甲小组设计的实验装置如下图,B中盛装的是吸收少量SO2的NaOH溶液,D中盛装的是1 mol·L-1 NaOH溶液。请回答下列问题: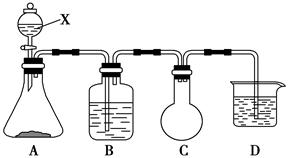
Ⅰ.
(1)写出仪器X的名称:________。
(2)写出A中发生反应的化学方程式:__________________________________。
(3)C装置的作用是_________________________________________________。
(4)D装置中反应的离子方程式:__________________________________。
(5)甲小组通过该实验要验证Cl2的________(填“漂白性”、“还原性”或“氧化性”);乙小组认为甲小组设计的实验装置有缺陷,请你帮助甲小组完善该装置。即还要A和B装置间连接一个装有_____________的洗气装置。
Ⅱ.丙小组认为反应一段时间后,B装置溶液(强碱性)中肯定存在Cl-、OH-和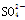 ,可能还含有其他的阴离子。请你帮助丙小组分析该吸收液中其他阴离子能否同时存在________(填“能”或“否”)。
,可能还含有其他的阴离子。请你帮助丙小组分析该吸收液中其他阴离子能否同时存在________(填“能”或“否”)。
高氯酸铵可用于火箭推进剂,实验室可由NaClO3等原料制取(部分物质溶解度如右图),其实验流程如下: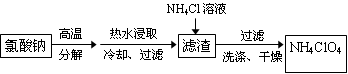
(1)氯酸钠受热分解生成高氯酸钠和氯化钠的化学方程式为。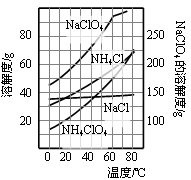
(2)滤渣的主要成分是(填化学式)。
(3)滤渣中加入氯化铵饱和溶液发生反应的离子方程式为。
(4)已知:2NH4ClO4 N2↑+2O2↑+Cl2↑+4H2O,现可提供下列试剂:
N2↑+2O2↑+Cl2↑+4H2O,现可提供下列试剂:
a.饱和食盐水b.浓H2SO4c.NaOH溶液d.Mge.Fef.Cu
利用下图装置(夹持装置略)对高氯酸铵热分解产生的三种气体进行分步吸收或收集。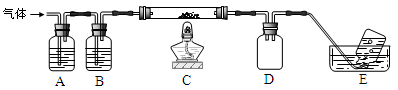
①E中收集到的气体可能是(填化学式) 。
②A、B、C中盛放的药品依次可以是、、(填字母序号)。
SO2和NOx都是大气污染物。
(1)直接排放含SO2的烟气会形成酸雨,危害环境。用化学方程式表示SO2形成硫酸型酸雨的过程。
(2)下表是某小组同学测得的不同天气情况下的某县城空气中SO2的平均含量。请你分析雨后或风速较大时SO2平均含量较低的原因:①雨后:___________;②风速较大时:_________。
(3)洗涤含SO2的烟气。以下物质不能作为洗涤剂的是________(填字母序号)。
a.熟石灰b.纯碱 c.CaCl2 d.NaHSO3
(4)煤燃烧前需进行脱硫处理,某种脱硫技术的基本原理如下: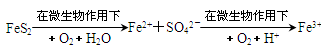
①该技术的第一步反应的离子方程式为。
②处理1 kg含80% FeS2的黄铁矿,第二步消耗O2(标况)的体积为L(保留一位小数)。
(5)某研究性学习小组为模拟光化学烟雾的形成,用紫外线照射装在密闭容器内的被污染空气样品,所得物质的浓度随时间的变化如图所示。由图可知,光化学烟雾是指等污染物气体和颗粒物所形成的烟雾。
(6)氧化—还原法消除NOx的转化如下: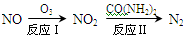
①反应Ⅰ为NO+O3=NO2+O2,生成11.2 L O2(标况)时,转移电子的物质的量是mol。
②反应Ⅱ中,当n(NO2)∶n[CO(NH2)2]=3∶2时,反应的化学方程式是。
(7)利用氨水可以将SO2和NO2吸收,原理如下图所示: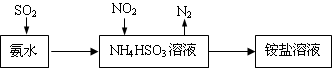
NO2被吸收的离子方程式是。
由短周期元素组成的中学常见物质A、B、C、D、E存在右图转化关系(部分生成物和反应条件略)。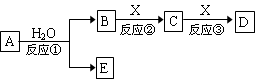
(1)若反应①在常温下进行,且E有漂白、杀菌作用,C是造成温室效应的主要气体,则:
E的电离方程式为,反应③的离子反应方程式为。
(2)若反应①是重要的工业反应之一, X是生产生活中使用最广泛的金属,则:
a.若B为气体单质,反应①的化学反应方程式为。
b.若E为非金属氧化物,C的化学式为。
(3)若A分子含有4个碳原子,D、E是同种有机物,75% B的水溶液常用于医疗消毒,则:反应①的化学反应方程式为。
(4)若A由两种元素构成,B为气体,E为白色沉淀,B、E都能使酚酞试液变红,则:反应①的化学反应方程式为。
Ⅰ.向FeCl3溶液中加入铁粉和铜粉混合粉末,充分反应后,下列情况可能存在的是(填序号)
| 序号 |
溶液中的盐 |
固体不溶物的成分 |
| ① |
FeCl3、CuCl2 |
Fe、Cu |
| ② |
FeCl2、CuCl2 |
Cu |
| ③ |
FeCl2 |
Cu |
| ④ |
FeCl3、CuCl2 |
Cu |
| ⑤ |
FeCl2、CuCl2 |
Fe |
| ⑥ |
FeCl2、CuCl2、FeCl3 |
没有固体不溶物 |
| ⑦ |
FeCl2 |
Fe、Cu |
Ⅱ.今有一包铁粉和铜粉混合粉末,为确定其组成,现提供4mol/L的FeCl3,溶液(其他用品略),某课外活动小组同学的实验结果如下(假定反应前后溶液体积不变)。
| 组别 |
① |
② |
③ |
④ |
| 混合粉末质量/g |
40 |
40 |
40 |
40 |
| V[FeCl3(aq)]/mL |
150 |
300 |
330 |
350 |
| 反应后剩余固体质量/g |
23.2 |
6.4 |
2.56 |
x |
(1)试判断第④组剩余固体质量x为。第①组实验中,发生反应的离子方程式为。
(2)试判断第②组剩余固体的成分为。
(3)原混合粉末中Fe、Cu的物质的量之比为。