(10分)某学生称取一定量的淀粉溶于水,测定淀粉的水解程度:
(1)各步所加试剂为:
A__________________;B__________________ ;C_____________________。
(2)淀粉水解产物的名称为:_____________,常用银镜反应实验或它与氢氧化铜悬浊液的反应来检验其存在。
(3)加碘水的作用是__________________________________,但是在加入B以后的混合液中,再滴入碘水溶液并未显出蓝色,此时能否说明淀粉水解完全?______________
理由是_____________________________________________________________________。
(4)关于水解反应下列叙述不正确的是( )
| A.糖类、油脂、蛋白质都能发生水解反应 |
| B.酯的水解反应是酯化反应的逆反应 |
| C.水解反应属于取代反应 |
| D.油脂在碱性条件下的水解反应称为皂化反应 |
在水溶液中,YO3n-和S2-发生反应的离子方程式如下:
YO3n- + 3S2- + 6H+=Y- + 3S↓+ 3H2O
(1)YO3n-中Y的化合价是,n=;
(2)Y元素原子的最外层电子数是。
(1998年上海)氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下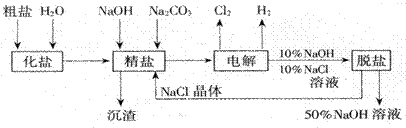
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为,与电源负极相连的电极附近,溶液pH(选填“不变”“升高”或“下降”)。
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为
、。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以
是(选填a,b,c多选扣分)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为有效除去Ca2+、Mg2+、SO42—,加入试剂的合理顺序为(选填a、b、c多选扣分)
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过、冷却、(填写操作名称)除去NaCl
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为。
请写出五种化学性质不同的物质的化学式,这些物质的原子核外都具有10个电子,它们的化学式分别为、、、、。
对一份白色固体,经过初步分析得知,其含有Na2CO3、Na2SO4、NaCl、CuSO4等物质中的一种或几种。甲乙两位同学为了进一步确定这份白色固体的组成成份而进行了如下实验,但实验中的有些问题还需你来作答。
(1)甲取少量白色固体在试管内用水溶解,结果得无色澄清的液体。因此,甲说肯定有一种物质不存在。这种物质的化学式是:______________
(2)甲又先后向那试管内加入了稍过量的BaCl2溶液和稀硝酸,结果是先产生了白色沉淀,后又有一部分沉淀消失并从溶液里冒出无色气泡。因此甲又说肯定有两种物质存在。这两种物质是:______________、_____________。
(3)乙将甲所得混合物进行了过滤,取滤液约2ml盛于另一支洁净的试管里,然后又向该试管内加入了稍过量的AgNO3溶液和稀硝酸,结果也产生了白色沉淀。因此乙说那份白色固体中也肯定有NaCl。你说乙的结论(填“对”或“不对”)__________,理由是:________________
、
、
、
、
是短周期元素,周期表中
与
、
与
相邻;
与
的最外层电子数之比为2∶3,
的最外层电子数比
的最外层电子数少1个;常见化合物
与水反应生成
的单质,且溶液使酚酞试液变红.
(1)
的元素符号是.
(2)
、
、
的氢化物稳定性顺序为(用分子式表示);
的氢化物和
的最高价氧化物的水化物反应生成
,则
中的化学键类型为,
的晶体类型为;
离子的电子式为.
(3)由
、
、
形成化合物的水溶液显碱性,其原因是(用离子方程式表示).
(4)一定量的
与
反应后的固体物质,恰好与0.8
稀盐酸溶液完全反应,并收集到0.25
气体,则用物质的量表示该固体物质的组成为.