可逆反应2NO2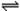 2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是( )
2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n molO2的同时生成2n mol NO2
②单位时间内生成n molO2的同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
| A.①④⑥ | B.②③⑤ | C.①③④ | D.①②③④⑤ |
下列化学方程式书写正确,且能用离子方程式Ba2++CO32-=BaCO3↓表示的是
| A.Ba(OH)2+CO2=BaCO3↓+H2O |
| B.Ba(HCO3)+Ba(OH)2 = 2BaCO3↓+2H2O |
| C.Ba(NO3)2+ Na2CO3= BaCO3↓+2NaNO3 |
| D.Ba(OH)2+ 2KHCO3 = BaCO3↓+KOH+H2O |
下列有关实验室制取气体的反应中,其原理不属于氧化还原反应的是
| A.实验室中用稀硫酸与锌粒反应制取H2 |
| B.实验室中用高锰酸钾加热分解制取O2 |
| C.实验室中用浓盐酸与二氧化锰加热制取Cl2 |
| D.实验室中用稀盐酸与石灰石反应制取CO2 |
已知某酸性溶液中含有Ba2+,则下述离子组中还能大量共存的是
| A.CO32-、Cl- | B.NO3-、Cl- | C.NO3-、SO42- | D.OH-、NO3- |
下列化学反应中,属于氧化还原反应的是
| A.Na2CO3+BaCl2===BaCO3↓+2NaCl |
| B.2AgNO3+Cu===Cu(NO3)2+2Ag |
C.2NaHCO3 Na2CO3+CO2↑+H2O Na2CO3+CO2↑+H2O |
| D.Na2O+H2O===2NaOH |
氧化还原反应在生产、生活中具有广泛的用途。下列生产、生活中的事例不属于氧化还原反应的是
| A.金属冶炼 | B.燃放鞭炮 | C.食物腐败 | D.点制豆腐 |