一定量某物质的溶液,其质量分数为0.2A,当加入等体积的水稀释后,其质量分数小于0.1A,则该溶液的密度 ( )
| A.大于水的密度 | B.小于水的密度 | C.等于水的密度 | D.无法确定 |
NA为阿伏加德罗常数,下列说法正确的是
| A.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
| B.标准状况下,22.4 L NH3中含有电子数为8NA |
| C.1 mol Cl2与足量Fe反应转移电子数为3NA |
| D.1 mol·L-1的AlCl3溶液中, Cl-的数目为3NA |
材料与化学密切相关。下列物质与材料对应关系不正确的是
| A.晶体硅——光导纤维 | B.氧化铝——耐火材料 |
| C.铁碳合金——碳素钢 | D.硅酸盐——普通玻璃 |
下列反应中,水作还原剂的是
| A.2Na+2H2O=2NaOH+H2↑ | B.Cl2+H2O=HCl+HClO |
| C.2F2+2H2O=4HF+O2 | D.SO2+H2O=H2SO3 |
下列离子在酸性溶液中能大量共存的是
A.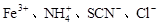 |
B.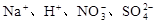 |
| C.Al3+、Fe2+、NO3-、Cl- | D.K+、Na+、Cl-、SiO32- |
下列离子方程式书写正确的是
| A.向氯化铝溶液中加入足量氨水:Al3+ + 4NH3·H2O ="=" AlO2- + 2H2O +4NH4+ |
| B.AlCl3溶液中加入足量的氨水:Al3++3OH-===Al(OH)3↓ |
| C.三氯化铁溶液中加入铁粉:Fe3++Fe===2Fe2+ |
| D.FeCl2溶液跟Cl2反应:2Fe2++Cl2===2Fe3++2Cl- |