(选做题)图表法、模型法是常用的科学研究方法。
I.下图是研究部分元素的氢化物的沸点变化规律的图像。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线——折线a和折线b(其中A点对应的沸点是100℃),你认为正确的是 ,理由是 。
II.人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属则被科学家预测为是钛(Ti)。钛被誉为“未来世纪的金属”。试回答下列问题:
(1)22Ti元素基态原子的价电子层排布式为 。
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,价电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如右图,则它的化学式是 。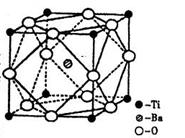
III.上世纪60年化,第一个稀有气体化合物Xe[PtF6]被合成出来后,打破了“绝对情性”的观念。在随后的几年内,科学家又相继后成了氙的氟化物、氧化物等。
(1)金属Pt内部原子的堆积方式与铜及干冰中的CO2相同,右图正方体是Pt晶胞的示意图,试说出Pt原子在晶胞中的位置 。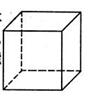
(2)稀有气体(氡除外)中,只有较重的氙能合成出多种化合物,
其可能原因是 (填字母代号)
| A.氙的含量比较丰富 | B.氙的相对原子质量大 |
| C.氙原子半径大,电离能小 | D.氙原子半径小,电负性大 |
(3)已知XeO3分子中氙原子上有1对弧对电子,则XeO3为 分子(填“极性”或“非极性”)。
有FeCl3和AlCl3的混合溶液100ml,向其中加入过量的NaOH溶液,充分反应后,过滤,干燥,共生成沉淀10.7g。
(1)写出混合溶液中加入过量NaOH溶液的离子方程式、;
(2)将10.7g沉淀加热灼烧,最后得到固体克;
(3)FeCl3的物质的量的浓度是mol/L;
(4)在加入NaOH溶液的过程中,生成沉淀的质量与加入NaOH溶液的体积如下图所示,计算AlCl3的物质的量的浓度mol/L;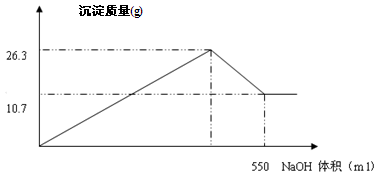
(5)求NaOH溶液的物质的量浓度?(提示:请写出第(5)小题的解题过程)
在一定条件下,用普通铁粉和水蒸气反应,可以得到铁的氧化物,该氧化物又可以经此反应的逆反应,生成颗粒很细的铁粉。某校化学小组利用下图所列装置进行铁与水反应的实验,并利用产物进一步与四氧化三铁反应制取铁粉。(装置中的铁架台、铁夹等必要的夹持仪器在图中均已略去)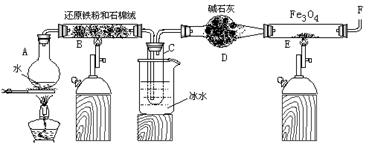
(1)烧瓶A中常加入碎瓷片,其作用是,B中石棉绒的作用,小试管C的作用是。
(2)反应开始时先点燃处(填A或B)酒精灯,为了安全,在E管中的反应发生前,在F出口处必须,E管中的反应开始后,在F出口处应。
(3)写出高温下Fe 与H2O(g)反应的化学方程式,在一定条件下该反应实际上是可逆反应,试用化学平衡移动原理加以解释本实验中是如何实现Fe向Fe3O4的转变的。
(4)停止反应,待B管冷却后,取其中固体加入过量稀盐酸,充分反应后过滤。简述证明滤液中含有Fe3+的实验操作及现象____________________________________________________。
粉末状试样A是由等物质的量的MgO和Fe2O₃组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20克A全部溶于0. 15L 6mol·L -1的盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12L气体(标准状况),同时生成溶液D,还有残留固体物质B;
④用KSCN溶液检验时,溶液D不变色。
请填空:
(1)①中引发铝热反应的实验操作是,
产物中的单质B是。
(2)②中所发生的各反应的化学方程式是、。
(3)③中所发生的各反应的离子方程式是、。
(4)若溶液D的体积仍视为0.15L,则该溶液中c(Mg2+)为,c(Fe2+)为。
有一块铝铁合金,将其溶于足量盐酸中,再加入过量氢氧化钠溶液,在空气中静置至红褐色沉淀不再增加为止,将沉淀滤出再灼烧至恒重,得到残留固体的质量与原合金的质量相同,则:
(1)合金溶于足量盐酸所得溶液中含有的阳离子有、、;
(2)沉淀滤出再灼烧至恒重,得到残留固体的化学式为;
(3)将沉淀滤出后所得的滤液中存在的阴离子有、、;
(4)合金中铝的质量分数为 。
实验室常用硫酸铝溶液和氨水反应制取氢氧化铝,其离子方程式为;
溶液中得到的氢氧化铝是______色______状物质。它是______溶于水的______性化合物,既能与______反应,又能与______反应,其离子方程式分别是、。