某化学反应的反应物和产物如下:
KMnO4 + KI+ H2SO4→ MnSO4 + I2 + KIO3 + K2SO4 + H2O
(1)该反应的氧化剂是 。
(2)如果该反应方程式中I2和KIO3的化学计量数都是5
①KMnO4的化学计量数是 。
②在下面的化学式上标出电子转移的方向和数目
KMnO4 + KI + H2SO4 →
(3)如果没有对该方程式中的某些化学计量数作限定,可能的配平化学计量数有许多组。原因是 。
市面上消毒剂、漂白剂的种类繁多。
(1)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只发生了氧化反应的是。(填序号)
a.MnO2b.KMnO4溶液 c.稀盐酸 d.Na2SO3溶液
(2)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,会发生如下的分解,配平反应的离子方程式,并用单线桥标出电子转移的方向和数目:
HClO2 ——ClO2↑+H+ +Cl-+H2O
该反应中氧化剂与还原剂的质量之比为:。若有标准状况下11.2 L的ClO2生成,则转移的电子数是。
(3)氧化物X是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由NaClO3和Na2SO3按物质的量比2:1,并在H2SO4存在的条件下加热制得,则X为, 请写出相应的离子方程式。
右图为实验室某浓盐酸试剂瓶的标签上的有关
数据,试回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为mol/L。
若用KMnO4氧化上述 HCl。其反应方程式如下:
2KMnO4+16HCl(浓)=2KCl+2MnCl 2+5Cl 2↑+8H2O
(2)该反应中的氧化剂是、氧化产物
是。
(3)1mol KMnO4完全反应,被还原的HCl的物质的量为mol。
(4)8mol HCl完全反应,产生的Cl 2在标准状况下的体积为升。
实验室利用右图所示装置进行NaHCO3的受热分解实验。请回答: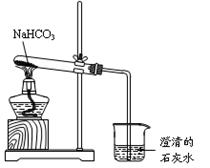
(1)加热一段时间后,烧杯中观察到的实验现象是 __。
(2)实验结束时的正确操作是(填序号)
① 先将导管从液体中移出,再熄灭酒精灯
② 先熄灭酒精灯,再将导管从液体中移出
(3)NaHCO3受热分解的化学方程式是___________
(4)若加热5.00 g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了0.31g,则原混合物中碳酸钠的质量为_____________________克。
在潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可用于制取氧气。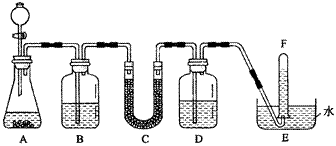
(1)A是用CaCO3制取CO2的装置。写出A中发生反应的化学方程式:
。
(2)按要求填写表中空格:
| 仪器编号 |
盛放的试剂 |
加入该试剂的目的 |
| B |
饱和NaHCO3溶液 |
|
| C |
与CO2反应,产生O2 |
|
| D |
吸收未反应的CO2气体 |
(3)为了达到实验目的,(填“需要”或“不需要”)在B装置之后增加一个吸收水蒸气的装置;若你认为需要增加一个吸收水蒸气装置,应选用作为吸水剂;若你认为不需要,请说明理由是。
(4)证明收集到的气体是氧气的方法是。
7分)某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下:(写出最佳答案)
(1)写出沉淀的化学式:沉淀1,白色沉淀2,
沉淀3;
(2)写出混合液加入A的离子方程式
(3)溶液加入B的离子方程式
已知:
| 溶解度 |
 |
C1- |
OH- |
| Ba2+ |
不溶 |
可溶 |
可溶 |
| Cu2+ |
可溶 |
可溶 |
不溶 |
| Ag+ |
微溶 |
不溶 |
不存在 |