同温同压下,同体积的NH3和H2S气体的质量之比为 ____ ;同质量的氨气和硫化氢气体的体积之比为 ___ ;若二者氢原子数相等,则它的体积之比为 __ 。
(14分) 能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH1 反应II:CO(g)+2H2(g)
CH3OH(g)+H2O(g)ΔH1 反应II:CO(g)+2H2(g) CH3OH(g)ΔH2
CH3OH(g)ΔH2
①上述反应符合“原子经济”原则的是(填“Ⅰ”或“Ⅱ”),
②下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)的变化
| 温度 |
250℃ |
300℃ |
350℃ |
| K |
2.041 |
0.270 |
0.012 |
I.由表中数据判断ΔH2 0(填“>”、“<”或“=”),
Ⅱ.若容器容积不变,下列措施可增加甲醇产率的是,
A.升高温度 B.将CH3OH(g)从体系中分离 C.使用合适的催化剂 D.充入He,使体系总压强增大 E.按原比例再充入 CO和 H2
Ⅲ.某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)="0.2" mol·L-1,则CO的转化率为,此时的温度为(从上表中选择);
(2)某实验小组依据甲醇燃烧的反应原理,设计如上图所示的原电池装置。
①该电池工作时,OH-向_______极移动(填“正”或“负”),
②该电池负极的电极反应为。
已知 ,有机玻璃可按下列路线合成:
,有机玻璃可按下列路线合成:
试写出:
(1) A、E的结构简式分别为:、。
⑵写出下列转化的化学方程式:
C→D;
G+F→H。
(8分) 根据下面的反应路线及所给信息填空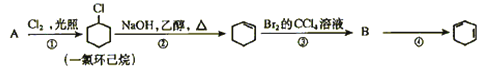
(1)A的结构简式是
(2)①的反应类型是。③的反应类型是。
(3)反应④的化学方程式是。
具有水果香味的中性物质A可以发生下列变化: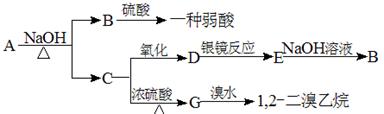
(1) 推断下述物质的结构简式:
A:________________ B:________________
C:________________ D:________________
(2) 写出下列变化的化学方程式:
A+NaOH→B+C:_____________________________________________
C→G:_________________________________________________
D→E:_________________________________________________
已知:①丙烯与水进行加成反应,其可能的产物有两种;②下图中E为开链的酯类化合物,其分子式为C6H12O2。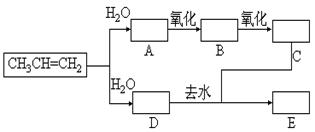
(1)请依据上述件和图中转化关系,写出化合物的结构简式。
AE
(2)D和浓HBr微热生成有机物F,写出有关反应的化学方程式
D+C→E的方程式:
B与新制银氨溶液反应的方程式: