双氧水(H2O2)是一种极弱电解质,也是一种“绿色氧化剂”。为了贮存、运输的方便,工业上将其转化为固态过碳酸钠(2Na2CO4·3H2O),该物质具有Na2CO3与H2O2的双重性质。请回答下列问题:
(1)写出H2O2的电子式: ,并写出它与SO2反应的化学方程式 。
(2)若把H2O2看成二元弱酸,写出它在水中第一步电离的方程式 。
(3)下列物质不会使过碳酸钠失效的是
| A.MnO2 | B.NaHCO3 | C.H2S | D.CH3COOH |
(4)稀H2SO4不与Cu反应,但在稀H2SO4中加入H2O2后则可使Cu溶解,写出该反应的化学方程式,并用单线桥标明电子转移的方向和数目。
(5)H2O2成为“绿色氧化剂”的理由是 。
某有机物A的相对分子质量为62。为进一步测定A 的化学式,现取6.2 g A完全燃烧,得到二氧化碳和水蒸气。将产物先后通过足量的浓硫酸和碱石灰,两者分别增重5.4 g和8.8 g(假设每步反应完全)。
(1)该有机物的实验式是 ________________;分子式是 ______________。
(2)红外光谱显示有“C—C”键和“O—H”键的振动吸收,若核磁共振氢谱只有2个吸收峰且峰面积之比为1∶2,推断该有机物的结构简式是 _______________________。
(3)该有机物与金属钠反应的化学方程式是______________________________________。
短周期主族元素A、B、C、D、E、的原子序数依次增大,A和B形成5个原子核的分子,A和C形成3个原子核的分子,且两种分子均含有10个电子。D的原子半径最大,A、B、D、E与C形成的化合物均有两种,其中E与C形成的化合物中的一种能使品红溶液褪色。
则由A、B、C三种元素组成的中学常见的化合物中:
①甲燃烧则其耗氧量与乙烯相同则甲的结构简式是。
②若乙能发生银镜反应则乙的化学式或结构简式是。
③若丙分子中的B、A、C最简个数比为1:2: 1且丙能与D发生反应,则丙的结构简式
④若丁标况下蒸汽密度为3.93g/L,B%=54.5%,A%=9.1%,且丁能发生水解反应则丁的结构简式为。
⑤若戊在同条件下密度为H2的22倍,4.4g该物质完全燃烧产物依次通过浓硫酸增重3.6g,碱石灰增重8.8g则戊的结构简式为。
下图为原电池的示意图。请回答: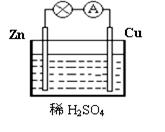
(1)Zn极为原电池的(填“正”或“负”)极,该极的电极反应式是,属于(填“氧化反应”或“还原反应”)。
(2)(填“电子”或“电流”)从锌片通过导线流向铜片,溶液中的H+从(填“锌片”或“铜片”)获得电子
写出下列反应的方程式 (1)乙烯可使溴的四氯化碳溶液褪色,该反应方程式为,
(1)乙烯可使溴的四氯化碳溶液褪色,该反应方程式为,
(2)苯与液溴在催化剂条件下反应的化学方程式为。
(3)写出苯与氢气反应反应方程式
有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大,已知A和C原子最外层只有一个电子,C燃烧时的焰色反应是黄色,C的单质在高温下与B的单质充分反应可以产生淡黄色固态化合物,A单质与D单质可以发生化合反应,且反应条件可以是点燃或者光照,试根据以上叙述回答:
写出A、B、C、D的元素名称:A _______ B _______ C _______ D ______。