已知卤代烃在氢氧化钠溶液中可以发生如下反应: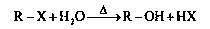
某芳香烃A有如下七步转化,按要求填空: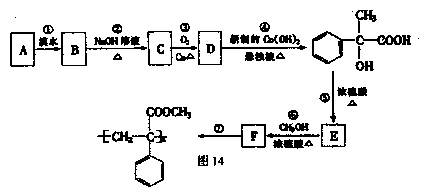
(1)写出反应类型:反应① ;反应⑦
(2)写出结构简式:A ;F
(3)写出化学方程式:
反应③
反应⑤
(1)氢化物的易燃性:第二周期__________>__________H2O>HF;
第三周期SiH4>PH3>__________>__________。
(2)化合物的毒性:PH3>NH3 H2S_______H2O;CS2__________CO2 CCl4>CF4(选填>或<)。
于是科学家们开始把注意力集中在含F、Cl的化合物上。
(3)已知CCl4的沸点为76.8℃。CF4的沸点为-128 ℃。新致冷剂的沸点范围介于其间。经过较长时间反复试验,一种新的致冷剂氟里昂CF2Cl2终于诞生了,其他类似的还可以是___________。
(4)然而,这种致冷剂造成了当今的某一环境问题是___________。但求助于周期表中元素及其化合物的___________变化趋势来开发致冷剂的科学思维方法是值得借鉴的。
①毒性②沸点③易燃性④水溶性⑤颜色
a.①②③ b.②④⑤c.②③④
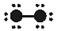
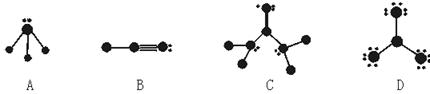
根据各图表示的结构特点,写出该分子的化学式:
A:B:C:D:
(2)在分子的结构式中,由一个原子提供成键电子对而形成的共价键用“→”表示,例如:
 |
硫酸写出三硝酸甘油酯的结构式:
。
为了测定乙醇的分子结构,有人设计了下图所示的用无水乙醇与钠反应的实验装置和测定氢气体积的测量装置,可供选用的实验仪器如下: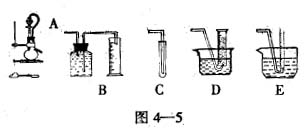
(1)测量气体体积的正确装置是(填写编号)
(2)装置中A部分的分液漏斗与蒸馏烧瓶间连接的导管所起的作用是(填写编号)
(A)防止无水酒精挥发
(B)保证实验装置不漏气
(C)使无水酒精容易滴下
(3)实验前先将小块钠在二甲苯中熔化成钠珠,冷却后倒入烧瓶中。其目的是。
(4)已知无水酒精的密度为0.789gcm-3,又2.Oml酒精反应完全后(钠过量),收集气体39Oml。则乙醇分子中能被钠取代出的氢原子为,由此可确定乙醇的结构式为而不是。
(5)实验所测定的结果偏高。可能引起的原因是(填写编号)
(A)本实验在室温下进行,
(B)无水酒精中混有微量甲醇
(C)无水酒精与钠的反应不够完全
BGO是我国研制的一种闪烁晶体材料,曾用于诺贝尔奖获得者丁肇中的著名实验,它是锗酸铋的简称。若知:①在BGO中锗处于最高价态,②在BGO中,铋的价态与铋跟氯形成某种共价氯化物时所呈的价态相同,在此氯化物中铋具有最外层8电子稳定结构③BGO可看成是由锗和铋两种元素的氧化物所形成的复杂氧化物,且在BGO晶体的化学式中,这两种氧化物中所含氧的总质量相同,请填空:
(1)锗和铋的元素符号分别是和
(2)BGO晶体的化学式是
(3)BGO晶体中所含铋的氧化物的化学式是。
A、B、C是在中学化学中常见的3种化合物,它们各由两种元素组成,甲、乙是两种单质,这些化合物和单质之间存在如下的关系:
单质甲 化合物A
化合物A 化合物B
化合物B 化合物B
化合物B
化合物A和化合物C单质乙和化合物C
据此判断:
(1)在A、B、C这3种化合物中,必定含有乙元素的是(用A、B、C字母填写)
(2)单质乙必定是(填“金属”或“非金属”),其理由是。
(3)单质乙的分子式可能是,则化合物B的分子式是