下列叙述正确的是
①热稳定性:H2O>HF>H2S ②熔点:Al>Na>K
③IA、IIA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤元素的非金属性越强,其氧化物的水化物酸性就越强
⑥已知2H2(g)+O2(g)=2H2O(l);△H=-571KJ·mol-1,则氢气的燃烧热为285.5KJ·mol-1
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P > N
A.只有②④⑥ B.只有①⑥⑦ C.只有②③④ D.只有③⑤⑦
若NA表示阿佛加德罗常数的值,据报道,科学家已成功合成了少量N4,
有关N4的说法正确的是()
| A.N4和N2是互为同位素 | B.1mol N4分子含有28NA个电子 |
| C.相同质量的N4和N2所含原子个数比为2:1 | D.N4的摩尔质量是56g |
我国稀土资源丰富。中国改革 开放的总设计师邓小平同志曾经意味深长地说:“中东有石油,我们有稀土。”。下列有关稀土元素
开放的总设计师邓小平同志曾经意味深长地说:“中东有石油,我们有稀土。”。下列有关稀土元素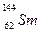 与
与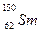 的说法正确的是()
的说法正确的是()
.
A.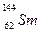 与 与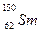 互为同位素 互为同位素 |
B.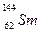 与 与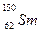 的质量数相同 的质量数相同 |
C.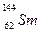 与 与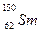 是同一种核素 是同一种核素 |
D.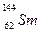 与 与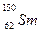 的核外电子数和中子数均为62 的核外电子数和中子数均为62 |
已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I━、Br━的溶液中通入适量氯气,溶液中各种离子的物质的量变化如下图所示。横、纵坐标的单位均为mol。
有关说法不正确的是()
| A.线段BC代表Fe3+ 物质的量的变化情况 |
| B.原混合溶液中c(FeBr2)= 6 mol/L |
| C.当通入Cl22mol时,溶液中已发生的反应可表示为:2Fe2++2I━+2Cl2=2Fe3++I2+4Cl━ |
| D.原溶液中n (Fe2+): n (I━): n(Br━)=2:1:3 |
下列叙述中正确的是 ()
()
| A.将盛有12mL NO2和O2的混合气体的量筒倒立于水槽中,充分反应后还剩余2 mL 无色气体,则原混合气体中O2的体积是4 mL 或 1.8mL |
| B.含a mol Na2CO3的溶液和含1.5a mol HCl的稀盐酸,无论正滴和反滴,生成的CO2相等 |
| C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应.在同温同压下,生成的CO2体积相同 |
| D.含a mol AlCl3的溶液和含1.5a mol NaOH的溶液,无论正滴和反滴,生成的 |
Al(OH) 3的质量相等
根据下表信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
| 主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
A.Q的氢化物比T的氢化物稳定且沸点高
B.同等条件下,L、R的单质与等浓度稀盐酸反应的速率为R>L
C.M与T形成的化合物具有两性
D.L、Q形成的简单离子的核外电子数相等