(1)某芳香烃的分子式为C8H10,它的一氯代物有二种,则其结构简式为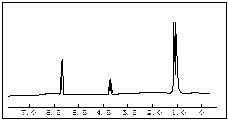
 (2)环己烷(C6H12)有12种结构,其中含三元环(三角形)的有 种。
(2)环己烷(C6H12)有12种结构,其中含三元环(三角形)的有 种。
(3)在 分子中,处于同一平面上的原子最多有
个。
(4)化合物A和B的分子式都是C3H8O,A的核磁共振氢谱图如左图所示,并且峰面积比分别为
1:1:6,
则A的结构简式为 。
甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料。以CH4和H2O为原料制备甲醇和二甲醚的工业流程如下: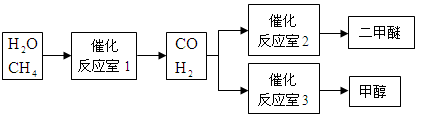
根据要求回答下列问题:
(1)“反应室1”在一定条件下反应的化学方程式为。
(2)水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g)ΔH= -90.8kJ·mol-1
CH3OH(g)ΔH= -90.8kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g)ΔH= -23.5kJ·mol-1
CH3OCH3(g)+H2O(g)ΔH= -23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g)ΔH= -41.3kJ·mol-1
CO2(g)+H2(g)ΔH= -41.3kJ·mol-1
完成热化学反应方程式:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g);ΔH=。
CH3OCH3(g)+CO2(g);ΔH=。
T ℃时,在容积为0.5 L的密闭容器中发生某一反应,且测得不同时间容器中四种物质A、B、C、D的物质的量变化如图所示。
已知:物质A、B、C均为气态、D为固态,正反应是吸热反应。根据要求回答下列问题:
(1)容器中反应的化学方程式为。
(2)前2 min,v(A)=______________ mol·(min·L)-1。
(3)能说明该反应已达到平衡状态的是___________。
A.混合气体的压强不变
B.混合气体的密度不变
C.消耗0.1mol的B同时生成0.1mol的D
D.B的物质的量不变
(4)T ℃时,该反应的平衡常数K=_________________(保留小数点后两位)。
(5)反应达到平衡后,改变下列措施能使A的转化率增大的是________(填选项字母)。
A.只增加A的物质的量 B.移走一部分D
C.升高反应体系的温度 D.把容器的体积缩小一倍
某研究性学习小组欲由硫铁矿烧渣(主要成分为Fe、Fe2O3、SiO2、Al2O3)制备绿矾(FeSO4·7H2O)并测定烧渣中铁元素的含量,流程图如下:
(1)操作a的名称是。
(2)加入足量试剂X后,发生反应的离子方程式为、。
(3)向溶液2中滴加KSCN溶液,无明显现象。向固体中加入足量稀硫酸后,发生氧化还原反应的离子方程式是、。
(4)硫铁矿烧渣中铁元素的质量分数为。
A~G是中学化学常见物质,其中A为相同条件下密度最小的气体单质,E为红棕色气体。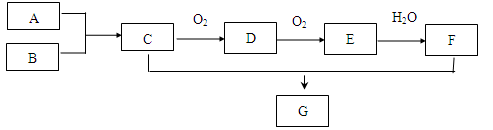
(1)G的化学式是。
(2)A和B反应生成C的化学方程式为。
(3)检验C可选用的试剂是(填字母)。
a.湿润的蓝色石蕊试纸 b.湿润的红色石蕊试纸 c.浓盐酸
(4)将盛满气体E的大试管倒扣在盛水的水槽中,发生反应的化学方程式为,现象为。
(5)汽车尾气中含有CO和物质D,一种治理方法是在汽车排气管上装一个催化转化装置,使CO和D反应,生成另外两种无毒气体。该反应的化学方程式是。
Na2CO3和NaHCO3是两种常见的钠盐。
(1)下列关于Na2CO3和NaHCO3性质的说法中,正确的是___________(填字母)。
a.常温下,Na2CO3在水中的溶解度比NaHCO3小
b.Na2CO3溶液和NaHCO3溶液均显碱性
c.可用Ca(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液
d.等物质的量的Na2CO3和NaHCO3分别与足量盐酸反应,在相同条件下产生CO2的体积相同
(2)实验室利用下图所示装置进行Na2CO3和NaHCO3热稳定性对比实验。请回答:
物质A是(填化学式),写出其中一种物质受热分解的化学方程式。
(3)若要除去碳酸氢钠溶液中的碳酸钠,请用化学方程式表示除杂原理。