A、B、C、D、E、F的原子序数依次增大,它们都具有相同的核外电子层数。已知:A、C、F三种原子最外层共有11个电子,且这三种元素原子的最高价氧化物对应水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素的符号:A ,B ,E 。
(2)把B的单质(片状)放入滴有酚酞的沸水中,观察到的现象是 ,反应的化学方程式是 。
(3)A、C两种元素的最高价氧化物对应水化物反应的离子方程式是 。
A与B反应生成C,假定反应由A、B开始,它们的起始浓度均为1 mol.L-1。反应进行2min后,A的浓度为0.8 mol.L-1 ,B的浓度为0.6 mol.L-1 C的浓度为0.6 mol.L-1
(1)2min内反应的平均反应速率为: ν(A)=
(2)ν(A)、ν(B)、ν(C) 三者之间的关系是:
(3)该反应的化学反应方程式:
根据下列反应的焓变,计算C(石墨)与H2(g)反应生成1molC2H2(g)的焓变(△H)。
C(石墨)+ O2(g)=CO2(g)△H1="a" kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H2="b" kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3="c" kJ·mol-1
△H=。
某研究性学习小组探究Na与CO2的反应,设计了如下装置进行探究。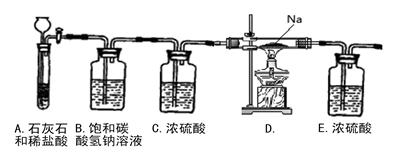
(1)从试剂瓶中取出的金属钠,须经过必要的操作,方可进行后续的实验,该必要的操作是。该装置B中饱和碳酸氢钠溶液的作用是,装置E中浓硫酸的作用是
(2)放进玻璃管中的金属钠在加热之前,必须先打开活塞,通入CO2, 这样操作的原因是
(3)用酒精灯给玻璃管加热,Na在充满CO2气体的玻璃管里剧烈地燃烧,产生大量的白烟。玻璃管中有黑色物质生成。玻璃管冷却后,玻璃管壁上附着一层白色物质。将玻璃管内物质转移至烧杯中, 加水,白色物质溶解于水,黑色物质不溶。过滤,得到澄清的滤液。往滤液中加CaCl2溶液,溶液变白色浑浊;再滴入稀盐酸,溶液中有气泡出现,则玻璃管壁上附着的白色物质是。另将滤纸上的黑色物质干燥,点燃,其燃烧产物无色无味且能使澄清石灰水变浑浊,则玻璃管中的黑色物质是。
(4)Na与CO2的反应的方程式为
将大豆油进行如下图所示的实验操作,请据此回答以下问题: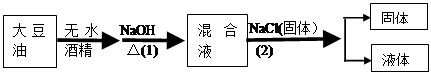
(1)该实验操作第(1)步中,化学反应类型为,检验该反应是否完全的方法是
(2)该实验操作第(2)步中,加固体NaCl的作用是,所得固体的主要用途是
某有机物A分子的球棍模型(最小球代表氢原子,其它球分别代表氧原子,碳原子和氮原子)如右图所示,请据此填空: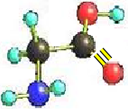
(1)A分子式具有官能团的名称
(2)A名称
(3)A和氢氧化钠溶液反应的离子方程式(A写结构简式)