(1)下列物质中,属于强电解质的是 (填序号,下同),属于弱电解质的是 ,属于非电解质的是 。
| A.NH4Cl | B.CaCO3 | C.SO2 | D.蔗糖 E、NaCl溶液 |
F、NaHCO3 G、NH3·H2O H、液氯 I、铜
(2)0.3 mol B2H6(气态高能燃料)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ 的热量,写出该反应的热化学方程式
。
(3)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l)
ΔH1=-870.3 kJ/mol
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ·mol-1
③H2(g)+O2(g)===H2O(l)ΔH3=-285.8 kJ·mol-1
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式
(7 分)某消毒液的主要成分为 NaClO(混有少量NaCl),请用相应的化学用语来解释下列事实。
(1)该消毒液可用NaOH 溶液吸收Cl2 制备,化学方程式为 。
(2)该消毒液的pH 约为12,离子方程式为 。
(3)向FeSO4溶液中滴入少量该溶液,溶液颜色变成棕黄色,反应的离子方程式为 。
(4)该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。每产生1 mol Cl2(标准状况下),转移电子个数约为 。
(8分)有A、B、C三种无色溶液,它们分别为葡萄糖溶液、蔗糖溶液、淀粉溶液中的一种,经实验可知:
①B能发生银镜反应;②A遇碘水变蓝色;③A、C均能发生水解反应,水解液均能发生银镜反应。
(1)试判断它们各是什么物质:
A是________,B是________,C是________。
(2)分别写出A、C发生水解反应的化学方程式:
A__________________________________
C:________________________________。
已知乳酸的结构简式为 。试回答:
。试回答:
①乳酸分子中含有________和_________两种官能团(写名称);
②乳酸与足量金属钠反应的化学方程式为___________________;
(6分)根据结构对有机物进行分类,有助于对其性质的掌握。
①下列有机物属于芳香烃的是 (填字母),
a. b.
b.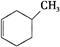 c.
c.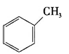
②下列有机物属于羧酸类的是 (填字母)。
a.CH3CHOb.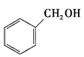 c.
c.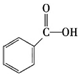
③下列有机物属于糖类的是 (填字母)。
a.油脂b.纤维素c.蛋白质
已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
(1)A分子中官能团的名称是 ,反应①的化学反应类型是 反应。
(2)反应④的化学方程式是 。
(3)某同学用如图所示的实验装置制取少量乙酸乙酯。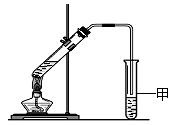
实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
①实验开始时,试管甲中的导管不伸入液面下的原因是 。
②若分离出试管甲中该油状液体需要用到的仪器是________(填序号)。
a.漏斗 b.分液漏斗 c.长颈漏斗
③实验结束后,若振荡试管甲,会有无色气泡生成,其主要原因是 (结合化学方程式回答)。