有一混合气体,可能由H2、O2、NH3、N2、CO2、HCl和He中的两种或多种组成。常温下,取此气体200mL进行实验,实验的过程和结果如下:
(1)观察此混合气体为无色。
(2)将此气体通过浓H2SO4,气体体积减少了40mL。
(3)将(2)中剩余的气体,通过Na2O2固体,气体体积变为120mL。
(4)将(3)中剩余的气体引燃充分反应后,冷却至常温,气体体积又减少了105mL。
(5)又将(4)中剩余的气体通过炽热的铜网,气体的体积又减少了三分之一(上述气体的体积都是相同条件下测定的)。
根据上述实验,试推断:
(1)混合气体中肯定存在的气体是 ,它们的体积分别为
。
(2)混合气体中肯定不存在的气体是 。
(3)混合气体中可能含有的气体是 ,其体积共为
。
要防止酸雨的产生,最直接的方法是阻止二氧化硫排放到空气中。回收二氧化硫的方法很多,常见的有石灰石及氨水法等,请大家根据原理写出反应的化学方程式。
(1)石灰石脱硫:
(2)氨水脱硫:
下表是某食品包装袋上的说明,从表中的配料中分别选出一种物质填在相应的横线上。
| 品 名 |
浓缩菠萝汁 |
| 配 料 |
水.浓缩菠萝汁.蔗糖.柠檬酸.黄原胶.甜蜜素.维生素C,菠萝香精.柠檬黄.日落黄.山梨酸钾等 |
| 果汁含量 |
≥80% |
| 生产日期 |
标于包装袋封口上 |
其中属于着色剂的有 ,属于调味剂的有 ,属于防腐剂的有 。
丙烯是石油化工的重要原料,一定条件下可发生下列转化:
已知: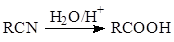

(1)A的结构简式为:;
(2)反应④的类型为:反应;
(3) D与足量乙醇反应生成E的化学方程式为:。
(4) 与足量NaOH溶液反应的化学方程式为。
与足量NaOH溶液反应的化学方程式为。
(5)B的同分异构体有多种.写出其中既能发生银镜反应,又能发生酯化反应的2种同分异构体的结构简式:、。
从某些植物树叶提取的挥发油中含有下列主要成分:
(1)写出A的分子式。
(2)1molB与溴水充分反应,需消耗mol单质溴。
(3)写出A与B在一定条件下相互反应,生成高分子化合物的化学方程式:
。
请写出 下列反应的化学方程式:
下列反应的化学方程式:
(1)氯乙烷在氢氧化钠水溶液中加热的反应:
(2)乙烯与水用硫酸作催化剂在加热条件下发生加成反应: