(1)在一定温度下,将2molA和2molB两种气体混合于2L密闭容器中,发生反应:3A(g)+2B(g) x C(g)+2D(g)ΔH <0 ,2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.2mol/L。由此推断:
x C(g)+2D(g)ΔH <0 ,2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.2mol/L。由此推断: ① x值等于 ; ② B的平衡浓度为 。
① x值等于 ; ② B的平衡浓度为 。 ③ A的转化率为 。
③ A的转化率为 。
④由于条件改变而引起反应速率和化学平衡的变化情况,a---b过程中改变的条件可能是 ;b----c过程中改变的条件可能是 ;之后若增大压强时,请把反应速率变化情况画在上图中的c-----d处(标明V正和V逆)该条件下反应建立新平衡后体系中混合气体的平均相对分子质量 (填“增大”或“减小”或“不变”)。
(选修—物质结构与性质)(12分)
X、Y、Z三种元素,原子序数依次增大,它们的原子序数之和为43。其中,Y原子的最外层电子数是次外层电子数的三倍。X、Y元素的单质都是构成空气的主要成分。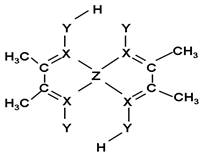
(1)Z原子的价层电子排布式为____________;XY3-离子的空间构型为__________。
(2)X单质与Y单质直接发生化合反应的化学方程式_________________________。
(3)ZO(氧化物)、FeO晶体结构类型均与NaCl的相同,Z2+和Fe2+离子半径分别为69pm和78pm,则熔点ZO_____FeO(填“<”或“>” )。
(4)ZO晶体中Z2+的配位数为____________。
(5)化合物A常用于检验Z2+:在稀氨水介质中,A与Z2+
反应可生成鲜红色沉淀,其结构如图所示:
该结构中,碳碳之间的共价键类型是______(“σ键”
或“π键”);X与Z2+离子间形成的是配位键,在图
上标出配位键的电子给予的方向。
该结构中,Y原子与氢原子除了形成共价键外,
还可存在_______;
该结构中,碳原子的杂化轨道类型有_____;Y原子的杂化轨道类型为_____。
(选修—有机化学基础)
某有机化合物A的结构简式如图,回答下列问题: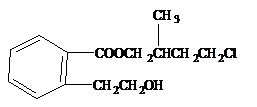
(1)A的分子式为。
(2)A在NaOH水溶液中加热得到B和C,C是
芳香族化合物, 则C的结构简式是。
(3)C酸化后可得F,F不能发生的反应类型是。 (填写字母代号)
a.取代反应 b.加成反应 c.消去反应 d.加聚反应 e.氧化反应 f.还原反应
(4)B与足量的某饱和一元羧酸D充分反应后生成E,E和B的相对分子质量之差为84,则D的摩尔质量为。
(5)F可以发生如下转化,且G与H互为同分异构体,G能生成高聚物。
请写出:①H的结构简式。 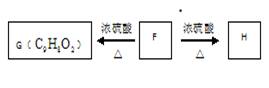
②由F生成G的化学方程式。
(6)符合下列三个条件的F的同分异构体的数目有多种,写出其中1种在同一个碳原子上连有两个不同的官能团的同分异构体的结构简式。
①含有邻二取代苯环结构 ②与F具有相同的官能团
③不与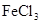 溶液发生显色反应
溶液发生显色反应
乙二酸(HOOC-COOH)俗名草酸,易溶于水,属于二元中强酸,在生产和科学实验中有着广泛的用途。草酸晶体的组成可用H2C2O4·xH2O表示,为了测定x值,进行如下实验:称取Wg草酸晶体,配成100.00mL水溶液,量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol·L-1的KMnO4溶液滴定,
(1)将所发生的反应方程式完成并配平,将完整的化学方程式写在答题卡上。 KMnO4 + H2C2O4+ K2SO4 + CO2↑+ MnSO4 +
KMnO4 + H2C2O4+ K2SO4 + CO2↑+ MnSO4 +
(2)整个实验过程中不需要的仪器有(填序号)。
a.托盘天平(带砝码,镊子)b.酸式滴定管 c.烧瓶 d.100mL容量瓶
e.烧杯 f.漏斗 g.锥形瓶 h.玻璃棒 i.药匙
(3)实验中,标准KMnO4溶液应盛装在____式滴定管中。滴定终点时溶液的颜色
变化为。
(4)在滴定过程中若用去amol·L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为________mol·L-1,由此可计算x的值是___________。(用含W、a、V的代数式表示)
(5)该小组同学将0.02mol草酸晶体(H2C2O4·2H2O)加入到100mL0.2mol/L的NaOH溶液中充分反应,测得反应后 溶液呈酸性,则该溶液中各离子浓度由大到小的顺序为。
溶液呈酸性,则该溶液中各离子浓度由大到小的顺序为。
甲醇是一种非常好的燃料。熔点-97.8°C,沸点64.5°C。一定条件下,
CO与H2反应可制得甲醇:CO+2H2 CH3OH
CH3OH
图1表示该反应进行过程中的能量变化:
图2表示100°C,在体积为2L的恒容容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。
(1)已知CO的燃烧热为283kJ/mol,H2的燃烧热为285.8kJ/mol,结合图1写出液态CH3OH燃烧热的热化学方程式。
(2)根据上图2计算:该温度下,反应CO(g)+2H(g) CH3OH(g)的平衡常数为;10min后,容器内的压强变为原来的倍;改变下列条件,能提高CO转化率的是。
CH3OH(g)的平衡常数为;10min后,容器内的压强变为原来的倍;改变下列条件,能提高CO转化率的是。
A.降低温度 B.加催化剂
C.充入氩气,使体系压强增大 D.再充入1molCO和2molH2
E.恒温恒容改为恒温恒压
(3)已知:CH3OH可以在一定条件下转化为HCOOH,HCOOH和CH3COOH性质相似。25°C,0.1mol/LHCOOH溶液的pH>1。室温下,向0.1mol/L的HCOOH溶液中滴加NaOH溶液,当溶液中离子浓度关系满足:c(HCOO-)<c(Na+)时,则反应的情况可能为。(填字母)
A.NaOH不足,HCOOH剩余
B.HCOOH与NaOH恰好完全反应
C.NaOH过量
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH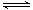 CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)常温常压下,在 pH =5的稀醋酸溶液中,c(CH3COO-)=_________(填数字表达式)。
下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是____(填字母)。
a.加入少量0.10 mol·L-1的稀盐酸 b.加热
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V盐酸______V醋酸 ,(填“>”、“<”或“=”下同),反应的最初速率为:υ盐酸_______υ醋酸。
(3)常温下,向体积为Va mL,pH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与Vb的关系是:_____________;溶液中各离子的浓度按照由大到小排序为_______。