下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A.D为金属单质,其他均为化合物.试回答下列问题: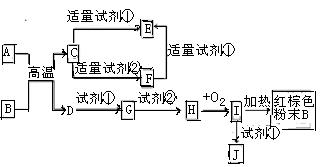
(1)写出物质C的化学式:
(2)写出物质B的一种用途:
(3)以J的饱和溶液制备胶体的操作为
 。
。
(4)写出下列反应的方程式:
A→F的离子方程式 .
H→I的化学方程式
试剂②可以由一种淡黄色固体粉末和一种常见液体发生反应而制得,其相应的化学方程式
(5)某同学认为J中可能同时含有同一种金属元素的两种阳离子,若要确认其中低价金属阳离子的存在,应选用 (选填序号)
A、KSCN溶液和氯水 B、铁粉和KSCN溶液 C、浓氨水 D、酸性高锰酸钾
苯佐卡因是一种局部麻醉剂,可用于粘膜溃疡、创面及痔疮的镇痛,一般制成软膏或栓剂合用。其合成路线如下图所示,其中有机物B具有酸性。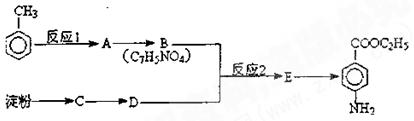
已知:①苯环上的取代反应有如下定位规律:当苯环上的碳原子连有甲基时,可在其邻位或对位上引入官能团;当苯环上的碳原子连有羧基时,可在其间位上引入官能团;
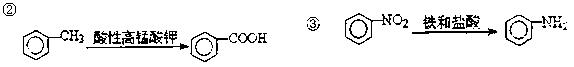
(1)反应类型:反应1 ;反应2 ;
(2)化合物A、C的结构简式:A ;C ;
(3)写出下列转化的化学方程式
C→D:
B+D→E:
(4)苯莽卡因有多种同分异构体,其中氨基直接连在苯环上,分子结构中含有-COOR官能团,且苯环上的一氯代物只有两种的同分异构体共有六种,除苯佐卡因外,其中三种的结构简式为: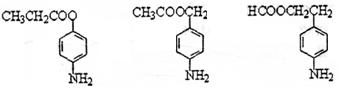
则剩余两种同分异构体的结构简式为: 、 。
实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜 色发生变化所用去的时间来判断空气中的含汞量,其反应为:
色发生变化所用去的时间来判断空气中的含汞量,其反应为:
4CuI+Hg==Cu2HgI4+2Cu、
(1)上述反应产物Cu2HgI4中,Cu元素显 价。
(2)以上反应中的氧化剂为 ,当有1molCuI参与反应时,转移电子 mol。
短周期的四种元素W、X、Y、Z,原子序数依次变小,四种元素的原子核外电子层数之和为8。X元素的原子最外层电子数等于Y和Z两元素的原子最外层电子数之和。W元素和Y元素的原子最外层上的电子数分别是各自电子层数的2倍。X和Z可以形成XZ3的化合物。
(1)写出元素名称:W__________,X____________,Y__________,Z__________。
(2)(XZ4)2W属于离子化合物,写出此化合物的电子式_________________。
(3)A物质是一种酸,它的一个分子里含有一个W原子,一个X原子,一个Y原子和一个Z原子, A物质的钾盐溶液常用检验___________(填写一种阳离子符号)。
(4)已知W、X、Y、Z四种元素可两两组成多种气态分子,其中两种可相互反应,且因量的不同而产物也不同,请写出其不同反应的化学方程式:①__________________________;
②___________________________________________________________________________。
(5)已知W、X、Y、Z四种元素可两两组成多种微粒,请写出其中所含电子数相同的任意三种微粒______________________________________。
下表是元素周期表的一部分,回答下列有关问题(用化学符号回答):
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
① |
② |
③ |
|||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
||
| 4 |
⑩ |
(1)在①~⑩元素中,最活泼的金属元素是,最活泼的非金属元素是,最不活泼的元素是。
(2)在①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是,碱性最强的是,呈两性的是。写出在水溶液中三者之间相互反应的离子方程式:,
,
。
用铜、银与硝酸银设计一个原电池,此电池的负极是:,
负极的电极反应式是:,
总反应方程式为。