(共12分)实验室中有甲﹑乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是碳酸钠溶液。为确定甲﹑乙两瓶溶液的成分及其物质的量浓度,现操作如下:
①量取25.00mL甲溶液,向其中缓缓滴加乙溶液15.00mL,共收集到CO2气体224mL﹙标况﹚。②量取15.00mL乙溶液,向其中缓缓滴加甲溶液25.00mL,共收集到CO2气体112mL﹙标况﹚。
请回答:
(1)根据上述两种不同操作过程及实验数据可判断甲溶液是 (填名称)
(2)甲溶液的物质的量浓度为 mol﹒L-1
乙溶液的物质的量浓度为 mol﹒L-1 ﹙忽略CO2在溶液中的少量溶解﹚。
(3)若用类似上述“互滴”的方式。
①将100 mL 3mol/L的NaAlO2溶液逐滴加到50mL12mol/L的HCl溶液中,充分反应。
写出发生反应的总反应离子方程式 。
②将50mL12mol/L的HCl溶液逐滴加入100 mL 3mol/L的NaAlO2溶液中,充分反应。两种混合方式生成沉淀的量是否相等 (填“相等”或“不相等”)
(13分)建筑工地常用的NANO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NANO2能发生如下反应:
(1)配平上述反应方程式。
(2)上述反应的氧化剂是;
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NANO2和NACl,可选用的物质有:
①水 ②碘化钾淀粉试纸 ③淀粉 ④白酒 ⑤食醋,进行实验,下列几组合适的是(填序号)。
| A.③⑤ | B.①②④ | C.①②⑤ | D.①②③⑤ |
(4)某厂废切削液中,含有2%~5%的NANO2,直接排放会造成污染,采用NH4Cl,能使NANO2转化为不引起二次污染的N2,反应的化学方程式为 ;该反应中被氧化的元素是。
下表是元素周期表的一部分。
已知A、B、C、D、E、X、Y是由表中给出元素组成的常见单质或化合物,并存在如图所示的转化关系(部分生成物和反应条件已略去):
(1)⑧的元素符号是。
(2)⑤与As两种元素中,非金属性较强的是(填元素符号)。
(3)用化学符号表示②⑤⑥⑦四种元素的简单离子半径由大到小是。
(4)元素③与②的最高价氧化物对应的水化物反应的化学方程式是______________。
(5)若A为红棕色气体,则A、X、D的化学式分别为、、。
(6)Y由②⑥⑦三种元素组成,它的水溶液是一种生活中常见的消毒剂。As可与Y的碱性溶液反应,当消耗1 mol还原剂时,消耗2.5 mol氧化剂,转移5 mol电子。该反应的离子方程式为。
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同。
回答下列问题:
(1)A与E形成的化合物的化学式是 。
(2)B的最高价氧化物化学式为,C的元素名称为 。
(3)D的单质与水反应的方程式为_。
(4)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是,有关反应的离子方程式为;。
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的电子式____________,结构简式____________。
(2)鉴别甲烷和乙烯的试剂是______(填序号)。
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是______(填序号)。
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
(4)已知 2CH3CHO+O2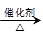 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示:
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如下图所示: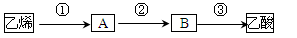
反应②的化学方程式为____________________________________。
工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为____________________________,反应类型是__________________。
A、B、C、D是原子序数依次增大的同一短同期元素,A、B是金属元素,C、D是非金属元素。
(1)A、B各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为____________________。
(2)A与C 可形成化合物A2C,该化合物的电子式为______________。
(3)C的低价氧化物通入D单质的水溶液中,发生反应的化学方程式为_______________。
(4)A、B、C、D四种元素简单离子的离子半径由大到小的顺序是(用离子符号表示):
_____>_____>______>______。
(5)四种元素中金属性最强的(填元素符号)______;非金属性最强的__________