二氧化碳是一种无色无味的气体,密度比空气大,可溶于水。通常实验室可以用碳酸钙(固体)和稀盐酸溶液来制取。如果是你要利用此反应原理制取二氧化碳气体你会选择跟 (填“过氧化氢”、“氯酸钾”)制取氧气相同的发生装置;收集方法可选用 ,收集后盖上玻璃片 (填“正放”、“倒放”)在桌上。
以下是对重要非金属及其化合物的讨论,根据要求回答问题:
(1)实验室盛装NaOH溶液的试剂瓶不能用玻璃塞,应该用橡胶塞,以防止发生反应: (离子方程式)。
(2)氨是一种重要的化工产品,密度比空气 (填“大”或“小”);工业上制备氨气的化学方程式为 。
(3)工业上制取漂白粉的化学反应方程式为 ;除去氯气中混有氯化氢的方法是将气体通入 溶液中。
(4)浓H2SO4常用作气体干燥剂,是因为它具有 ;将适量的蔗糖放入烧杯中,滴入几滴水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到 ;产生刺激性气味气体的化学方程式为 。
(5)铜和稀硝酸反应的离子方程式是 。若参加反应的Cu质量为6.4g,则转移电子物质的量为 mol。
以下是对重要金属及其化合物的讨论,根据要求回答问题:
(1)写出钠与水反应的离子方程式 ,Na2O2的用途之一是 。
(2)在AlCl3溶液中逐滴滴入过量的NaOH溶液,观察到的现象是 ,
反应的离子方程式为 , 。
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为 。
(4)刻蚀印刷电路板涉及的离子方程式为 ,检验Fe3+中混有Fe2+的试剂是 。
烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ·mol-1
NO(g)+1/2O2(g)=NO2(g) △H=-58.2kJ·mol-1
SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241.6kJ·mol-1
(1)反应3NO(g)+O3(g)=3NO2(g)的△H=_______mol·L-1。
(2)室温下,固定进入反应器的NO、SO2的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):n(NO)的变化见下图。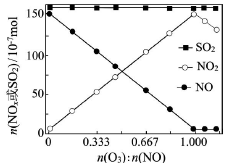
①当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是 。
②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是 。
(3)当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(pH约为8)中SO32-将NO2转化为NO2-,其离子方程式为: 。
(4)CaSO3水悬浮液中加入Na2SO4溶液,达到平衡后溶液中c(SO32-)= [用c(SO42-)、Ksp(CaSO3)和Ksp(CaSO4)表示];CaSO3水悬浮液中加入Na2SO4溶液能提高NO2的吸收速率,其主要原因是 。
某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)______________________.
(2)上述(B)操作的目的是______________________。
(3)上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是(填“偏大”、“偏小”或“不变”,下同)_________________________。
(4)实验中用左手控制滴定管活塞,眼睛注视______________________,直至滴定终点,判断到达终点的现象是: 。
(5)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对测定结果的影响是 。
(6)滴定结束后如仰视观察滴定管中液面刻度,则对滴定结果的影响是 。
甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+ 2H2(g) CH3OH(g) △H1=-116 kJ·mol-1
CH3OH(g) △H1=-116 kJ·mol-1
(1)下列措施中既有利于增大反应速率又有利于提高CO转化率的是_____________。
| A.随时将CH3OH与反应混合物分离 |
| B.降低反应温度 |
| C.增大体系压强 |
| D.使用高效催化剂 |
(2)在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律。右图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。请回答: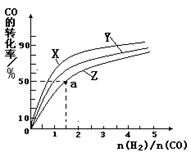
①在上述三种温度中,曲线Z对应的温度是
②利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+ 2H2(g)  CH3OH(g)的平衡常数 K= 。
CH3OH(g)的平衡常数 K= 。
(3)在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol•L-1)变化如下表所示:
| 0min |
5min |
10min |
|
| CO |
0.1 |
0.05 |
|
| H2 |
0.2 |
0.2 |
|
| CH3OH |
0 |
0.04 |
0.05 |
若5min~10min只改变了某一条件,所改变的条件是 ;且该条件所改变的量是