现用质量分数为98%、密度为1.84g·cm-3的浓H2SO4来配制500mL、0.2mol·L-1的稀H2S04。可供选择的仪器有:①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥容量瓶⑦托盘天平⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2S04时用不到的有 (填代号)。
(2)经计算,需浓H2S04的体积为 。现有①10mL②50mL③100mL三种规格的量筒,你选用的量筒是 (填代号)。
(3)将浓H2S04加适量蒸馏水稀释后,冷却片刻,随后全部转移到 mL的容量瓶中,转移时应用玻璃棒搅拌。转移完毕,用少量蒸馏水洗涤 2—3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度 处。改用 加蒸馏水到瓶颈刻度的地方,使溶液的 。 振荡、摇匀后,装瓶、贴签。
(4)在配制过程中,其他操作都准确,下列操作中:
错误的是 ,能引起误差偏高的有 (填代号)。
①洗涤量取浓H2S04后的量筒,并将洗涤液转移到容量瓶中 ②未等稀释后的H2S04溶液冷却至室温就转移到容量瓶中 ③将浓H2S04:直接倒人烧杯,再向烧杯中注入蒸馏水来稀释浓H2S04④定容时,加蒸馏水超过标线,又用胶头滴管吸出 ⑤转移前,容量瓶中含有少量蒸馏水 ⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线 ⑦定容时,俯视标线
写出下列物质的电子式
(1)SiF4
(2)C2H2
(3)NaOH
已知乙烯能发生以下转化:
(1)写出反应的化学方程式
①:反应类型:
②:反应类型:
③:反应类型:_________
(2)丙烯与乙烯的关系是,丙烯发生加聚反应的方程式是_________
下面列出了几组物质,请将物质的合适组号填写在空格上。
同位素,同素异形体,同分异构体。
①刚石与“足球烯”C60;
②D与T;
③16O、17O和18O;
④氧气(O2)与臭氧(O3);
⑤CH4和CH3CH2CH3;
⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);
⑦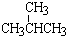 和
和 ;
;
⑧ 和
和  ;
;
写出电极反应式:
(1)钢铁的吸氧腐蚀
正极:;负极:。
(2)氢氧燃料电池(稀硫酸作电解质)
正极:;负极。
热化学方程式:
(1)在标准状况下的11.2L甲烷完全燃烧生成CO2和液态水放出444.8KJ热量(298K),其热化学方程式为。
(2)已知断裂下列1mol化学键需要吸收的能量分别为:C="O:745KJ/mol" , O="O:496kJ/mol" , C-H:414KJ/mol 则断裂1molH-O键需要提供的能量为kJ