右图是用自来水制取少量蒸馏水的简易装置,(加热及固定仪器略),其原理与教材中的实验完全相同。回答下列问题:
⑴加热左边大试管前要向其中加入 ,其作用是 ;
⑵该装置中使用的玻璃导管较长,其作用是 ;
⑶烧杯中还要盛有的物质是 。
现要配制500mL2.0mol/L的NaOH溶液,请填写下列空白:
(1)若用固体NaOH作溶质,需NaOH的质量为 ,称取这些NaOH常用的仪器有;
(2)若用10mol/L的NaOH溶液作溶质,需NaOH溶液的体积为,量取该NaOH溶液常用的的仪器有;
(3)从上述配制的溶液中取出10mL,其中NaOH的物质的量浓度为,含有NaOH的质量为;
(4)将取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为。
某待测液中可能含有A13+、Fe3+、K+、NH4+、C1-等离子,现通过如下实验对其中的阳离子进行检验:
(1)取少量待测液,仔细观察,呈无色;
(2)向上述待测液中滴加NaOH溶液,有白色沉淀生成,NaOH溶液过量后沉淀又完全溶解,再加热还有刺激性气味的气体产生,该气体能使湿润的红色石蕊试纸变蓝。
据此可以判断该待测液中一定含有的阳离子是,一定没有的阳离子是。还有一种阳离子没有检验,检验这种离子的实验方法是(填写实验名称),现象是。
某固体化合物A,按下图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色。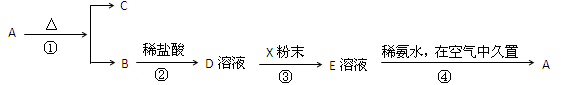
(1)请写出下列物质的化学式:A、C。
(2)在①②③④各步反应中属于氧化还原反应的有(填序号)。
(3)请分别写出反应①的化学方程式和反应③的离子方程式:①、③。
有A、B、C、D四种含硅元素的物质,它们能发生如下反应:
①C与烧碱反应生成A和水;②A溶液与钙盐溶液反应生成白色沉淀D;
③B在空气中燃烧生成C;④C在高温下与碳反应生成单质B。
根据上述变化,完成下列问题:
(1)写出B、D的化学式:B、D。
(2)写出C与烧碱反应的化学方程式:。
写出A溶液与钙盐溶液反应的离子方程式:。
【化学—选:3:物质结构与性质】 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物,其晶胞结构如右图。
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物,其晶胞结构如右图。 请回答:
请回答: (1)A元素的名称是;
(1)A元素的名称是; (2)B元素原子核外运动状态不同的电子数为,C元素原子价电子层的电子排布图为,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是
(2)B元素原子核外运动状态不同的电子数为,C元素原子价电子层的电子排布图为,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是 (3)元素E在周期表中的位置是,它的+2价离子的电子排布式为:
(3)元素E在周期表中的位置是,它的+2价离子的电子排布式为:
(4)由以上五种元素的任意两种形成的常见化合物中,所含离子键成分最多的可能为 (5) 如图所示,D跟B形成的离子化合物晶体的密度为ag·cm-3,则晶胞的体积是
(5) 如图所示,D跟B形成的离子化合物晶体的密度为ag·cm-3,则晶胞的体积是
(只要求列出算式)。