【化学—选:3:物质结构与性质】 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物,其晶胞结构如右图。
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物,其晶胞结构如右图。 请回答:
请回答: (1)A元素的名称是 ;
(1)A元素的名称是 ; (2)B元素原子核外运动状态不同的电子数为 ,C元素原子价电子层的电子排布图为 ,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是
(2)B元素原子核外运动状态不同的电子数为 ,C元素原子价电子层的电子排布图为 ,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是  (3)元素E在周期表中的位置是 ,它的+2价离子的电子排布式为 :
(3)元素E在周期表中的位置是 ,它的+2价离子的电子排布式为 :
(4)由以上五种元素的任意两种形成的常见化合物中,所含离子键成分最多的可能为  (5) 如图所示,D跟B形成的离子化合物晶体的密度为ag·cm-3,则晶胞的体积是
(5) 如图所示,D跟B形成的离子化合物晶体的密度为ag·cm-3,则晶胞的体积是
(只要求列出算式)。
A、B、C、D、E、F六种物质在一定条件下有下图所示的相互转化关系,所有反应物和生成物均已给出。试回答: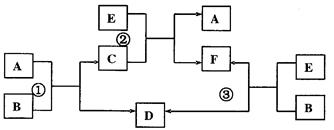
(1)若反应①、②、③均为溶液中进行的置换反应,A、D、E分别为铝、铁、铜三种金属中的一种,则A的元素符号为____________。请写出反应③的离子方程式:
________________________________________________________________。
(2)反应①、②、③均为在溶液中进行的复分解反应。A在常温下为无色刺激性气体,并能使湿润的红色石蕊试纸变蓝;E为常见碱,其焰色反应呈黄色;溶液中形成的D是白色沉淀,且具有两性。
若B能与硝酸银溶液反应产生白色沉淀,则B的化学式为____________________。
写出E与D反应的离子方程式____________________________________________。
(1)氢氧化铝Al(OH)3是一种治疗胃酸(含盐酸)过多的药物,请用化学方程式 表示该反应的原理:。
表示该反应的原理:。
(2)炒菜时,经常加入少量的料酒(含乙醇)和醋,可使菜变得香醇可口,主要是因为上述两种物质发生了某种反应,请用化学方程式表示该反应的原理:
。
(3 )醋还可用于除去热水瓶胆内的水垢(设其主要成分为碳酸钙),请用化学方程式表示该反应的原理:。
)醋还可用于除去热水瓶胆内的水垢(设其主要成分为碳酸钙),请用化学方程式表示该反应的原理:。
(4 分)
分)
(1)药物黄麻碱是从中药麻黄中提取的生物碱,可用于治疗支气管哮喘、鼻黏膜充血引起
的鼻塞等。服用麻黄碱的不良反应是有时会出现由于中枢兴奋所导致的不安、失眠等,
晚间服用最好同服镇静催眠药以防止失眠。麻黄碱的结构简式如图所示。
请写出麻黄碱的分子式__________________
(2)药物可分为处方药和非处方药。“OTC”表示____________________
从
| A.甲醛 | B.葡萄糖 | C.乙醇 | D.油脂等四种有机物中选择合适的答案,将其标号填在空格内。 |
(1)工业上制备肥皂的主要原料是 。
。
(2)家居装修材料中散发出的有毒物质是
(3)常用做燃料和医药上消毒剂的是
(4)糖尿病人通常是指病人的尿液中的含量高。
下表为元素周期表的一部分。表中所列的字母分别代表某一元素。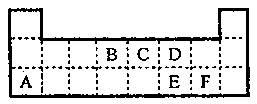
(1)元素F的名称是_____________;
(2)B、C、D、E四种元素的氢化物中最稳定的是____________(写化学式);
(3)写出B的最高价氧化物的电子式 ________;
(4)1molA与D的氢化物完全反应产生的气体在标准状况下的体积为。