如图所示,是一个制取氯气并以氯气为原料进行特定反应的装置,其中各试剂瓶装的试剂为:B(品红溶液)C(氯化亚铁溶液)D(碘化钾淀粉溶液)E(水)H(紫色石蕊试液)
(1)A是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其化学反应方程式是:
(2)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃G处酒精灯,回答下列问题:
下列装置中的现象是B ;D
请写出C和D中的化学方程式
C: D:
(3)在G装置的硬质玻璃管内盛有碳粉,发生氧化还原反应,一种产物能使H处紫色石蕊试液变红,另一产物能使澄清石灰水变浑浊,写出G中的反应的化学方程式 。
(4)在H处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是 。
(5)G处反应完毕后关闭分液漏斗旋塞,移去酒精灯,但由于余热的作用,A处仍有氯气产生,此时应该怎样操作 ;装置Ⅰ中的现象是 。
(6)若将E中的水换成氢氧化钠溶液,溶液中不但有NaClO还有NaClO3,其物质的量比为2:1,则氧化剂和还原剂的物质的量比为: 。
按要求用合适的化学用语填空
Ⅰ.在原子序数1—18号元素中:
(1)与水反应最剧烈的金属是_____________。
(2)与水反应最剧烈的非金属单质是_____________。
(3)原子半径最小的元素是_____________。
(4)气态氢化物最稳定的化学式是_____________。
(5)电子数为10的分子(写5个)
Ⅱ.下列各分子中,所有原子都满足最外层为8电子结构的是
①. H2O②. BF3③.CCl4④. PCl3⑤. SO3⑥. N2⑦. CO2
为扩大现有资源的使用效率,在一些油品中加入降凝剂J,以降低其凝固点,扩大燃料油品的使用范围。J是高分子聚合物,它的合成线路可以设计如下,其中A的氧化产物不发生银镜反应:
试写出:
(1)反应类型:abc
(2)结构简式:FH
(3)化学方程式:D→E
E+K→J
三种常见元素结构信息如下表,试根据信息回答有关问题:
| 元素 |
A |
B |
C |
| 结构信息 |
基态原子核外有两个电子层,最外层有3个未成对的电子 |
基态原子的M层有1对成对的p电子 |
基态原子核外电子排布为[Ar]3s104sx,有+1、+ 2两种常见化合价 2两种常见化合价 |
(1)写出B原子的基态电子排布式;
(2)用氢键表示式写出A的氢化物溶液中存在的氢键(任写一种);A的氢化物分子结合一个H+形成阳离子后,其键角(填写“变大”、“变小”、“不变”);
(3)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为,简要描述该配合物中化学键的成键情况;
(4)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“○”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。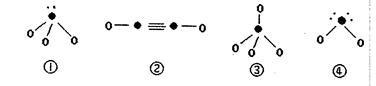
在以上分子中,中心原子采用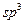 杂化形成化学键是(填写序号);在②的分子中有个
杂化形成化学键是(填写序号);在②的分子中有个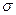 键和个
键和个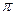 键。
键。
农作物生长不仅需要阳光、空气和水,还需要多种化学元素。当植物缺乏N元素时,表现为植株生长缓慢、叶色发黄,严重时叶片脱落直至死亡。
(1)下列可作氮肥的化合物是,其中含N量最高的是。
| A.硫酸铵 | B.磷酸二氢钙 | C.硫酸钾 | D.尿素 |
(2)氮肥的制备,首先涉及氨的合成,请填写下列合成氨工艺流程图中的设备名称:
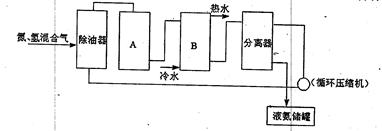
AB
(3)某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的合成氨厂联合设计了以下制备(NH4)2SO4的工艺流程: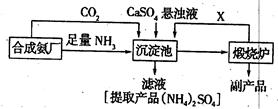
①沉淀池中发生的主要反应方程式是;
②在上述流程的沉淀池中通入足量氨气的目的是,可以循环使用的X是;
③从物质的性质和工业生产实际的角度考虑该流程的主要缺陷是。
(Ⅰ)某化学兴趣小组的同学得上用下 图所示实验装置进行实验(图中a、b、c表示止水夹)。
图所示实验装置进行实验(图中a、b、c表示止水夹)。
(1)请利用上述装置设计一个简单的实验验证Cl-和Br-的还原性强弱。
①选择合理的装置连接:→→(填字母编号)。
②选择所需的试剂:(填字母编号)。
a.固体氯化钠 b.固体二氧化锰 c.浓硫酸
d.浓盐酸 e.稀盐酸 f.溴化钠溶液
③实验现象及结论:。
(Ⅱ)电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收并制备NiSO4·7H2O晶体,设计实验流程如下: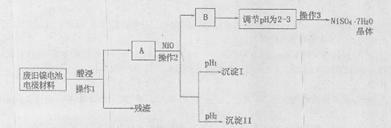
已知:①NiSO4易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的KSP及析出理论pH如下表所示:
| M(OH)n |
Ksp |
pH |
|
| 开始沉淀 |
沉淀完全 |
||
| Al(OH)3 |
1.9×10-23 |
3.43 |
4.19 |
| Fe(OH)3 |
3.8×10-38 |
2.53 |
2.94 |
| Ni(OH)2 |
1.6×10-14 |
7.60 |
9.75 |
回答下列问题:
(1)根据上表数据判断操作2依次析出的沉淀I是沉淀II是(填化学式),pH1pH2(填“>”、“<”或“=”);
(2)操作1和操作2所用到的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为。
(3)“调节pH为2-3”的目的是;
(4)NiSO4在强碱溶溶中用NaClO氧化,可制得碱性镍镉电池电极材料——NiOOH。该反应的离子方程式是。