(1)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25℃10kPa下,10g甲醇燃烧生成CO2和液态水时放热226.8kJ。请写出表示甲醇燃烧的热化学方程式:
(2) 某些化学反应可用下式表示:A + B  C + D + H2O
C + D + H2O
请回答下列问题:
①若A、D均可用于消毒,且C是家家户户的厨房必备的调味品之一,写出该反应的离子方程式 。
②若A为水垢的主要成分之一,B是日常生活常见有机物(厨房用品),
写出该反应的化学方程式: 。
③若C、D均为气体且都能使澄清石灰水变浑浊,则只用
或 (任写两种试剂的名称)就可以鉴别C、D两种气体。
根据要求填空:
(1)只用键线来表示碳架,两根单键之间或一根双键和一根单键之间的夹角为120˚,一根单键和一根三键之间的夹角为180˚,而分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略,而其他杂原子及与杂原子相连的氢原子须保留。每个端点和拐角处都代表一个碳。用这种方式表示的结构式为键线式。写出下列有机物的键线式:
①CH3(CH2)2COOH____________________;②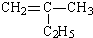 :__________________。
:__________________。
(2)写出下列原子团的电子式:①甲基 _______________;②氢氧根离子 _____________
(3)写出有机物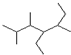 的名称 _______________________________________
的名称 _______________________________________
(4)在有机物分子中若某一个碳原子连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”.C7H16的同分异构体中具有“手性碳原子”的有 ___________种.
(5)某有机高分子化合物的结构片段如下: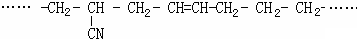
则合成它的单体是 ____________________________________。
从樟科植物枝叶提取的精油中含有下列甲、乙两种成分: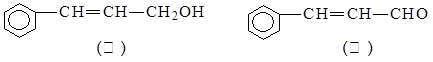
(1)乙中所含官能团的名称为;
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):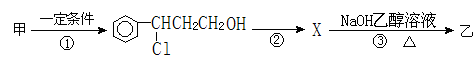
设计步骤①的目的是;指出①的反应类型;
反应②的化学方程式为(注明反应条件)。
(3)欲检验乙中的含氧官能团,选用下列的一种试剂是__________。
| A.溴水 | B.酸性高锰酸钾溶液 | C.溴的CCl4溶液 | D.银氨溶液 |
(4)乙经过氢化、氧化得到丙( )。写出同时符合下列要求的丙的同分异构体结构简式__________________、_________________
)。写出同时符合下列要求的丙的同分异构体结构简式__________________、_________________
①能发生银镜反应;②能与FeCl3溶液发生显色反应;③核磁共振氢谱图上产生4个吸收峰。
向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
(一)在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
(1)写出H2O的空间构型________。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是 。
| A.氧原子的杂化类型发生了改变 | B.微粒的形状发生了改变 |
| C.微粒的化学性质发生了改变 | D.微粒中的键角发生了改变 |
(3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞示意图(未按顺序排序)。与冰的晶体类型相同的是 (请用相应的编号填写)。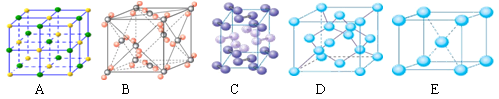
(二)胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上。
(4)写出铜原子价电子层的电子排布式 ,与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素是 (填元素符号)。
(5)实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有 ____ 。
(6)实验过程中加入C2H5OH后可观察到析出深蓝色[Cu(NH3)4]SO4·H2O晶体。实验中所加C2H5OH的作用是 ____________ 。
据新华社报道,发展改革委员会于2007年4月发出“遏制铝冶炼投资反弹”的紧急通知。原因是铝冶炼属高耗能产业,而且某些铝冶炼企业以污染环境为代价,得不偿失。
如图是传统的工业生产金属铝的基本流程图,阅读上述新闻信息,结合铝生产的流程图解答下列问题: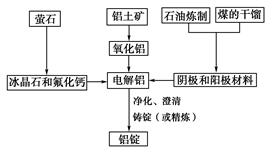
请回答:
(1)工业冶炼金属铝用的是铝土矿,铝土矿的主要成分是________(填化学式)。石油炼制和煤的干馏产品____________(填物质名称)作电解铝的阴极和阳极材料。
(2)氧化铝熔点高达2050 ℃,工业上为了降低能量消耗,在金属铝的冶炼中采取的措施是__________________________。
(3)在冶炼过程中,阳极材料需要定期地进行更换,原因是该极材料不断被消耗,产生这种现象的原因是:__________________________________________(用化学方程式表示)。
(4)工业上制取金属镁时是电解MgCl2,电解反应方程式为_________________,镁和铝都是活泼金属,为什么在电解冶炼过程中,一个用氯化物,一个用氧化物?原因是:
_________________________________________________________________。
下表为元素周期表的一部分,请参照元素①一⑧在表中的位置,用化学用语回答下列问题: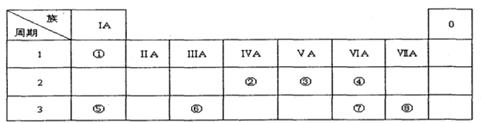
Ⅰ.(1)请画出元素⑧的阴离子结构示意图。
(2)④、⑤、⑦的原子半径由小到大的顺序为。
(3)⑤和⑥的最高价氧化物对应水化物的碱性强弱为>。
(4)④、⑤两种元素的原子按1:1组成的常见化合物的电子式为。
Ⅱ.由表中①一⑧中的一种或几种元素形成的常见物质A、B、C可发生以下反应(副产物已略去),试回答: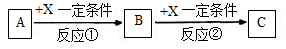
(1)若X是一种常见过渡金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的方法是;又知在酸性溶液中该金属离子能被双氧水氧化,写出该反应的离子方程式。
(2)若A、B、C为含有同一金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为,写出A与C两溶液反应的离子方程式____。