下列物质有如下转化关系(有的反应物生成物未列出),其中:D为碱,G为酸,金属甲在G的浓溶液中会钝化;F的溶液中只含一种溶质。
A、B、C、D,E均由Q,R、x、T四种短周期元素中的两种或三种组成,且Q、R、X、T原子序数依次增大;X的最外层电子数是电子层数的3倍;R和X相邻;Q和T同主族,Q为非金属元素,T为金属元素。则:
(1)X在周期表中的位置是 ,R、X、T的原子半径从小到大的顺序为
(用元素符号表示);
(2)A和G等物质的量反应产物的水溶液显 性,其原因用离子方程式表示为 ;
(3)A和X2反应的化学方程式为 ;
(4)为保护环境,通过安装汽车尾气处理装置,使尾气中的E和CO反应转化为两种空气的成分,当反应转移l mol电子时,生成的气体在标准状况下的总体积为 L。
磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池的电极材料。某化工厂以铁红、锂辉石LiAl(SiO3)2(含少量Ca2+、Mg2+的盐)、碳粉等原料来生产磷酸亚铁锂。其主要工艺流程如下:
已知:2LiAl(SiO3)2 + H2SO4(浓)  Li2SO4 + Al2O3·4SiO2·H2O↓
Li2SO4 + Al2O3·4SiO2·H2O↓
| 温度/℃ |
20 |
40 |
60 |
80 |
| 溶解度(Li2CO3)/g |
1.33 |
1.17 |
1.01 |
0.85 |
| 溶解度(Li2SO4)/g |
34.2 |
32.8 |
31.9 |
30.7 |
(1)从滤渣Ⅰ中可分离出Al2O3,如下图所示。请写出生成沉淀的离子方程式。
(2)滤渣Ⅱ的主要成分是:(填化学式)。
(3)向滤液Ⅱ中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是
。
(4)写出在高温下生成磷酸亚铁锂的化学方程式。
(5)磷酸亚铁锂电池总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应:。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为。
LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应:。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为。
1808年,英国化学家戴维用钾还原氧化镁,最早制得少量的镁。镁是航空工业的重要材料,镁合金用于制造飞机机身、发动机零件等,一架超音速飞机约有5%的镁合金构件,一枚导弹一般消耗100~200公斤镁合金;镁作为一种强还原剂,还用于钛、锆、铍和铀等的生产中;镁是燃烧弹和照明弹不能缺少的组成物;镁粉是节日烟花必需的原料。镁及其合金是一种用途很广泛的金属材料,目前世界上60%的镁是从海水中提取的。从海水(主要含NaCl和MgSO4)中提取金属镁的主要步骤如下:
回答下列问题:
(1)Mg在周期表中的位置______________________,试剂A可以选用_____________________,试剂C可选用_______________________;
(2)步骤①的离子方程式_________________________________________;
(3)用电子式表示氯化镁的形成过程_______________________________;
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为:_____________________________________________________;
(5)戴维制镁的化学方程式为_____________________________________;
(6)配平下列反应的方程式。
① 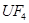 +
+  ——
——  +
+ 
②  +
+  ——
——  +
+ 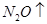 +
+ 
2011年5月1日起,《中华人民共和国刑法修正案(八)》正式实施,醉酒驾驶作为危险驾驶罪被追究驾驶人刑事责任。醉酒驾驶的界定标准为:每百毫升血液中的酒精含量高于或等于80毫克,相当于3两低度白酒或者2瓶啤酒。乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是含碳化合物,其中B是烃。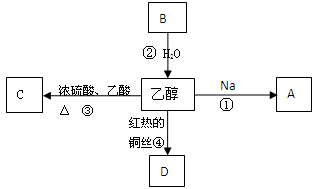
回答下列问题:
(1)物质B的电子式:,C的结构简式:。
(2)写出下列化学反应方程式及反应类型(有机物用结构简式):
反应①:,反应类型:。
反应②:,反应类型:。
反应③:,反应类型:。
反应④:,反应类型:。
(3)炒菜时,加一点酒和醋能使菜味香可口,原因是()
A.有盐类物质生成B.有醇类物质生成
C.有酯类物质生成D.有酸类物质生成
某温度时, 在一个0.5 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。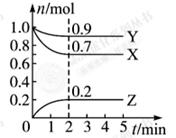
根据图中数据回答下列问题:
(1)该反应的化学方程式为。
(2)反应开始至2 min,以气体Z表示的平均反应速率为。
(3)用物质X表示的化学反应速率为0.2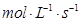 与用物质Y表示的化学反应速率为0.1
与用物质Y表示的化学反应速率为0.1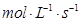 ,哪个快?()
,哪个快?()
a.前者 b.后者 c.一样快 d.无法比较
(4)若X、Y、Z均为气体,2 min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的倍;
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时(填“增大”“减小”或“相等”)。
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。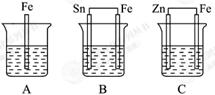
(1) A中反应的离子方程式为。
(2)B中Sn极的电极反应式为。Sn极附近溶液的c (填 “变大”“变小”或“不变”)。
(填 “变大”“变小”或“不变”)。
(3)C中被腐蚀的金属是,总反应的化学方程式为
,比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为(填序号)。