某温度时, 在一个0.5 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。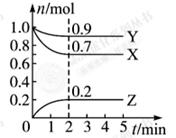
根据图中数据回答下列问题:
(1)该反应的化学方程式为 。
(2)反应开始至2 min,以气体Z表示的平均反应速率为 。
(3)用物质X表示的化学反应速率为0.2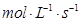 与用物质Y表示的化学反应速率为0.1
与用物质Y表示的化学反应速率为0.1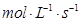 ,哪个快?( )
,哪个快?( )
a.前者 b.后者 c.一样快 d.无法比较
(4)若X、Y、Z均为气体,2 min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的 倍;
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时 (填“增大”“减小”或“相等”)。
某烷烃A,其蒸气密度是相同状况下氢气密度的64倍,经测定得知A分子中共含有6个甲基。
(1)若A不是烯烃与氢气加成的产物,则A的结构简式为:;
(2)若A是炔烃与氢气加成的产物,则A的名称为:。
露天烧烤不仅产生大量有害气体污染环境,而且在烧焦的肉类中还含有强烈的致癌物:苯并芘,其结构简式为:
(1)它是一种稠环芳香烃,其分子式为;
(2)此物质中碳元素和氢元素的质量比为。
有M、R、Q、V、W、X、Y、Z八种物质,它们之间存在如下关系:
①M+Y R②R+H2O→NaOH+Y③Q+NaOH→V+W+H2O④X
R②R+H2O→NaOH+Y③Q+NaOH→V+W+H2O④X W+Y
W+Y
⑤X+W+H2SO4 Q+Z+H2O。其中M、Q、Y是单质,Q、Y在常温、常压下为气体,Z是硫酸盐,钠、钾化合物性质相似。
Q+Z+H2O。其中M、Q、Y是单质,Q、Y在常温、常压下为气体,Z是硫酸盐,钠、钾化合物性质相似。
回答下列问题:
(1)写出各代号的化学式(或分子式) M, R,Q,V,W,X,Y,Z。
(2)写出下列有关化学反应的方程式和离子方程式,并标出电子转移方向和总数
反应③,;
反应⑤,。
(1)材料是人类赖以生存和发展的重要物质基础。
①住宅建设需大量的建筑材料,下列物质属于复合材料的是(填字母)。
a.水泥 b.PVC下水管道 c.玻璃 d.钢筋混凝土
②现代生活离不开金属材料,下列钢铁的防腐方法中,防腐效果最好,但相对费用也最贵的是(填字母)。
a.涂油漆 b.包塑料层(镀塑) c.制成不锈钢
③废品收购人员发现金属铝做的易拉罐“不生锈”,而铁生锈最厉害,便认为金属铁比铝性质活泼.你认为易拉罐“不生锈”原因是;用盐酸可除去铁尺上的铁锈(主要成分为Fe2O3),请您写出除去铁锈的化学方程式;
④废旧电池中含有汞,如果随意丢弃,会造成污染,威胁人类健康.汞的元素符号是,金属汞在常温下的状态是。常用的干电池内部填有氯化铵和二氧化锰等物质,在实验室分离氯化铵和二氧化锰混合物,可进行的操作是:溶解、过滤和;得到的氯化铵在农业上又可用作。
(2)2012年3月,新《环境空气质量标准》的颁布表明国家对环境问题的进一步重视。
①汽车上加装尾气催化净化装置可以使NO、CO相互反应转化为空气中含有的两种气体。名称分别为和。
②煤燃烧产生的SO2所形成的酸雨中,SO2最终转化成的酸是(填化学式)。在煤中加入适量石灰石,在氧气的共同作用下,可以与煤燃烧产生的SO2反应生成硫酸钙和二氧化碳气体,发生反应的化学方程式为。
(3)某种食品的配料标签如图所示。
| 配料: 小麦粉 淀粉 鸡蛋 棕榈油 碳酸氢钠 苯甲酸钠等 |
①该配料中,富含蛋白质的物质是,富含油脂的物质是。
②该配料中的具有防腐作用。
③请写出检验淀粉的实验方法和现象:。
下列说法正确的是。
①丙烷中三个碳原子在同一条直线上;②烃类分子中的碳原子通过形成四对共用电子对与其他原子结合;③乙醇分子中无碳碳双键,所以是饱和烃;④糖类、油脂、蛋白质均是由C、H、O三种元素组成的;⑤淀粉、纤维素、油脂、蛋白质均属于天然高分子化合物;⑥含5个碳原子的有机物,每个分子中最多可形成4个C—C单键;⑦所有的烃中碳原子与碳原子之间均是以碳碳单键相连;⑧ 表示苯的分子结构,其中含碳碳双键,因此苯的性质跟乙烯相似。
表示苯的分子结构,其中含碳碳双键,因此苯的性质跟乙烯相似。