(1)下列有关实验操作或判断不正确的是 。
| A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏小 |
| B.用干燥的pH试纸测定氯水的pH |
| C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌 |
| D.在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量 |
E.观察钾元素焰色反应的操作:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,观察.
F.制备氢氧化亚铁时,将盛有NaOH溶液的滴管,伸入硫酸亚铁溶液中
(2)除杂(括号内为杂质):请把所加试剂和有关离子反应方程式填在空白处。
| |
试剂 |
离子反应方程式 |
| ①NaHCO3溶液(Na2CO3) |
|
|
| ② Fe2O3(Al2O3) |
|
|
| ③FeCl3溶液(FeCl2) |
|
|
| ④CO2(HCl) |
|
|
A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A原子核内无中子;A和E、D和F分别同主族,且B与D 最外层电子数之比为2:3。试回答下列问题:
(1)A元素的名称是 ,E元素在周期表中的位置是 ;
(2)C、D、F的气态氢化物稳定性由强到弱的顺序是 (填化学式);
(3)E单质在足量D单质中燃烧生成的化合物的电子式是 ;
(4)化合物 X、Y均由A、D、E、F四种元素组成。
X、Y均由A、D、E、F四种元素组成。
①X、Y均属于 化合物(填“离子”或“共价”);
②X与Y的水溶液相混合发生反应的离子方程式为 ;
(5 )化合物E2F的水溶液中滴入双氧水和稀硫酸,加热,有单质生成。其离子反应方程式为: 。
)化合物E2F的水溶液中滴入双氧水和稀硫酸,加热,有单质生成。其离子反应方程式为: 。
(附加题)某气态烷烃和乙烯等体积混合时,1体积混合气体完全燃烧消耗同 温同压下4.75体积氧气。试回答:
温同压下4.75体积氧气。试回答:
(1)该烷烃的分子式为;
(2)该烷烃所有同分异构 体的结构简式为。
体的结构简式为。
已知乙烯能发生以下转化:
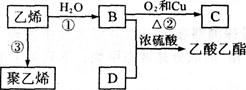
(1)乙烯的结构式为:_________________________。
(2)写出下列化合物官能团的名称:
B中含官能团名称___________;D中含官能团名称____________。
(3)写出反应的化学方程式及反应类型:
①______________________________________________;反应类型:________。
②_____________________________________________。
在2008 年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
 (1)该融雪剂的化学式是;Y的最高价氧化物的水化物中含有的化学键是。
(1)该融雪剂的化学式是;Y的最高价氧化物的水化物中含有的化学键是。 (2)元素D原子的最外层电子数是其电子层数的2倍,且D与Y相邻;E是短周期最活泼的金属元素,试用电子式表示D与E组成化合物的形成过程为。
(2)元素D原子的最外层电子数是其电子层数的2倍,且D与Y相邻;E是短周期最活泼的金属元素,试用电子式表示D与E组成化合物的形成过程为。 (3)元素W与Y同周期,其氧化物可作为太阳能电子板的材料;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是________ _________。
(3)元素W与Y同周期,其氧化物可作为太阳能电子板的材料;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是________ _________。 (4)W的氧化物是玻璃的主要成分,易与烧碱反应,该反应的化学方程式为:
(4)W的氧化物是玻璃的主要成分,易与烧碱反应,该反应的化学方程式为: _______________________ ______________________。
_______________________ ______________________。
(1)食物中的营养物质主要包括:糖类、_______、蛋白质、维生素、无机盐、__________。
(2)迄今为止,煤、石油、_____________仍是人类使用的主要能源,它们同属于化石能源,是不可再生能源,需要合理开发利用。
(3)淀粉在稀酸的催化作用下,能最终水解为葡萄糖,欲检验淀粉是否完全水解,可 以在水解反应混合物中滴加_______________溶液,通过溶液有没有发生显色反应来判断。
以在水解反应混合物中滴加_______________溶液,通过溶液有没有发生显色反应来判断。