某研究性学习小组为了测定某品牌合金中铝的含量,现设计了如下实验:
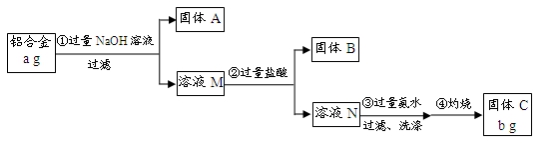
已知:(1)该铝合金的主要成分为铝、镁、铜、硅。
(2)常温下,硅能和NaOH发生反应:Si+2NaOH+H2O===Na2SiO3+2H2↑。
(3)硅酸不溶于水
(4)固体C为Al2O3
请回答下列问题:
(1)固体A在潮湿的空气中久置可能会发生一个明显的变化,这个变化是 ;发生反应的化学方程式为 ;
(2)步骤③中洗涤沉淀的实验操作为 ;
(3)该样品中铝的质量分数是 (用a、b表示);
(4)下列因操作不当,会使测定结果偏大的是 ;
A.第③步中沉淀未用蒸馏水洗涤
B.第①步中加入NaOH溶液不足
C.第④步对沉淀灼烧不充分
将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是 g)求:
(1)加入NaOH溶液0--20mL过程中反应方程式
为:_______________________。160--180mL过程中反应方程式为_______________________。
(2)合金中Mg的质量为____________g。所用HCl 的物质的量浓度为____________mol/L。
实验室中需要220mL0.5mol/L H2SO4,现用98%浓硫酸(密度为1.84g/cm3)稀释配制。
(1)本实验室中需要的仪器是。
(2)要将浓硫酸在中稀释,稀释时的操作方法是。
(3)必须将稀释后的硫酸后再移液,原因是,否则,所配制的稀硫酸浓度会(偏高、偏低、无影响)。
某无色透明溶液可能存在Na+、Fe3+、Ba2+、NO3-、CO32-、HCO3-、SO42-中的几种离子,现有如下操作:
Ⅰ、取适量该溶液加入CaCl2溶液无沉淀,继续滴加盐酸产生无色无味的气体。
Ⅱ、另取该溶液滴加一定量的NaOH溶液有白色沉淀生成。
试回答下列问题:
该溶液中一定存在的离子有______________,一定不存在的离子_____________。
用一个离子方程式表示操作②的实验现象:
________________________________________________________。
将总物质的量为4mol的Na2O2和Al2(SO4)3的混合物投入足量水中,充分反应后生成y mol沉淀(y>0)。若以x表示原混合物中Na2O2的物质的量,试建立y=f(x)的函数关系式,将x的取值和y=f(x)关系式填写在表内(可不填满,也可补充)。
| 序号 |
x值 |
y=f(x) |
| ① |
||
| ② |
||
| ③ |
||
| ④ |
已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体, C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。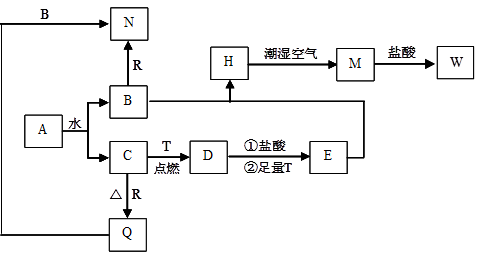
(1)写出下列物质的化学式:
A:D:R:。
(2)按要求写下列反应方程式:
H在潮湿空气中变成M的过程中的化学方程式:;
向N中通足量CO2时反应的离子方程式:;
D与盐酸反应的离子方程式:。
(3)简述检验气体C的方法:。