(8分)实验室也可用KMnO4固体和浓盐酸反应制氯气,反应方程式如下:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
完成下列问题:
(1)该反应中氧化剂是_____________;还原产物是_____________。
(2)若反应中有0.5 mol电子转移,被氧化的HCl的物质的量是多少?有多少克KMnO4参加了反应?
A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,E、E、F为同一周期,A与D,C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可心分解成Y,X的电子式为_______________,其分子属于________(填“极性”或“非极性”)分子。D与C形成的化合物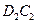 可与Y的应生成单质C,该反应的化学方程式为____________________。
可与Y的应生成单质C,该反应的化学方程式为____________________。
(2)E是非金属元素,其单质在电子工业中有重要应用,请写出工业生产单质E的化学反应程式:_____________________________。
(3)一定条件下,A的单质气体与B的单质气体充分反应生成W气体(已知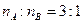 ),W的空间构型为_______________,工业上合成W气体选择的条件是________________。
),W的空间构型为_______________,工业上合成W气体选择的条件是________________。
(4)A的单质与C的单质在KOH的深溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入A的单质气体,N极通入C的单质气体,则M极的电极反应式为____________________________________。
(5)在10L的密闭容器中,通入2mol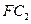 气体和3mol C的气体单质,一定条件下反应后生成
气体和3mol C的气体单质,一定条件下反应后生成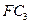 气体,当反应达到平衡时,单质C的浓度为
气体,当反应达到平衡时,单质C的浓度为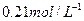 ,则平衡时
,则平衡时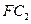 的转化率为________。
的转化率为________。
某种手液中含有PCMX,对革兰氏阳性和阴性菌及霉菌具有极好的杀灭效果。
(1)PCMX分子中含有苯环,相对分子质量为156.5,该有机物含有碳、氢、氧、氯四种元素,其中氯和氧元素的质量比为35.5︰16,则有机物的分子式是_______。
(2)PCMX分子的苯环上含有四个取代基,其中相同的两个取代基处于间位,另外两个不同的取代基处于对位;该有机物在一定条件下能跟浓溴水发生苯环上的取代反应,且PCMX与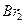 的物质的量之比为1︰2。PCMX结构简式是_________________,其中含氧官能团名称是__________________。
的物质的量之比为1︰2。PCMX结构简式是_________________,其中含氧官能团名称是__________________。
(3)PCMX在光照的条件下,跟氯气反应生成一氯代物的化学方程式是_____________________________________________。
(4)已知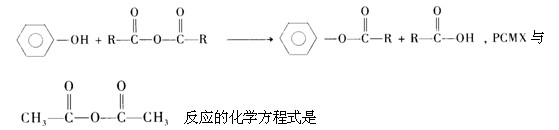
____________________________________________________________________
(5)PCMX的同分异构体中,有两个取代基,且能跟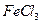 溶液发生显色反应的有________种,写出其中两种的结构简式________________,_________________。
溶液发生显色反应的有________种,写出其中两种的结构简式________________,_________________。
如图表示某因态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4︰5,化合物D是重要的工业原料。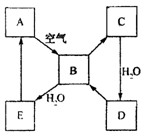
(1)写出A在加热条件下与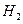 反应的化学方程式
反应的化学方程式
________________________________。
(2)写出E与A的氢化物反应生成A的化学方程式
_______________________________________________________________。
(3)写出一个由D生成B的化学方程式
_______________________________________________________________。
(4)将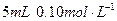 的E溶液与
的E溶液与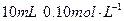 的
的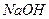 溶液混合。
溶液混合。
①写出反应的离子方程式_______________________________________________。
②反应后溶液的pH ___ 7(填“大于”、“小于”或“等于”),理由是_______________。
③加热反应后的溶液,其pH___(填“增大”、“不变”或“减小”),理由是_________。
现有pH=2的醋酸溶液甲和pH=2的盐酸乙,请根据下列操作回答问题:
(1)取10mL的甲溶液,加入等体积的水,醋酸的电离平衡_________移动(填“向左”,“向右”或“不”);其pH值变__________(填“增大”、“减小”或“无法确定”);另取10mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中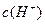 和
和 的比值将____________(填“增大”、“减小”或“无法确定”),其pH值变__________(填“增大”、“减小”或“无法确定”)
的比值将____________(填“增大”、“减小”或“无法确定”),其pH值变__________(填“增大”、“减小”或“无法确定”)
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为: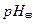 ______
______ (填“大于”、“小于”或“等于”)
(填“大于”、“小于”或“等于”)
(3)各取25mL的甲、乙两溶液,分别用等浓度的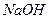 稀溶液中和至
稀溶液中和至 ,则消耗的
,则消耗的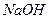 溶液的体积大小关系为:
溶液的体积大小关系为: ______
______ (填“大于”、“小于”或“等于”)
(填“大于”、“小于”或“等于”)
(4)取25mL的甲溶液,加入等体积 的
的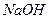 溶液,反应后溶液中
溶液,反应后溶液中 、
、 的大小关系为:
的大小关系为: ______
______ (填“大于”、“小于”或“等于”)
(填“大于”、“小于”或“等于”)
有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程图生产的。图中M和A都可发生银镜反应,N和M的分子中碳原子数相等,A的烃基上的一氯取代位置有三种。
试写出:
(1)物质的结构简式:A___________,M___________。
(2)反应类型:X____________,Y___________。
(3)物质A的同分异构体结构简式为:___________________________。(写出两个即可)。
(4)D→高分子涂料的化学方程式:___________________________。
(5)N+B→D的化学方程式:___________________________。