阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是 ( )
| A.常温常压下,18.0 g NH4+中所含的质子数为6.02×1024 |
| B.250mL2mol/L的氨水中含有NH3·H2O的分子数为0.5×6.02×1023 |
| C.1 L 1 mol/L的K2CO3溶液中离子总数大于3NA |
| D.1mol Cl2参加的任何反应,反应过程中转移电子数都是2NA |
根据下列实验现象,所得结论正确的是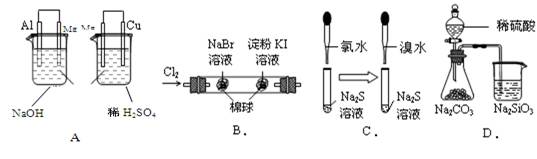
下列离子方程式正确的是
| A.FeCl3溶液中滴加过量Na2S溶液:2Fe3++S2—═2Fe2++S↓ |
| B.将Na2O2固体投入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ |
| C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使SO42—完全沉淀: NH4++Al3++2SO42—+2Ba2++4OH—= Al(OH)3↓+NH3·H2O+2BaSO4↓ |
| D.少量CO2通入苯酚钠溶液中:2C6H5O—+CO2+H2O = 2C6H5OH+CO32— |
已知NH4CuSO3与足量的1mol/L硫酸溶液混合微热,产生下列现象:
①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。
据此判断下列说法合理的是
| A.NH4CuSO3中硫元素被氧化 | B.刺激性气味的气体是二氧化硫 |
| C.刺激性气味的气体是氨气 | D.该反应中硫酸作氧化剂 |
进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习方法之一。下列对有关实验事实的解释正确的是
| A.燃着的镁条在二氧化碳气体中剧烈燃烧,生成白色粉末和黑色固体,说明镁燃烧时不能用二氧化碳灭火 |
| B.紫色高锰酸钾溶液中通入SO2后,溶液颜色褪去,说明SO2具有漂白性 |
| C.铜和浓硝酸反应生成NO2,铜和稀硝酸反应生成NO,说明稀硝酸的氧化性比浓硝酸强 |
| D.氢气在氯气中安静燃烧,发出苍白色火焰,说明氢气与氯气作用直接生成了挥发性的盐酸 |
某无色溶液中能大量共存的一组离子是
| A.OH-、Ba2+、HCO3-、Cl- | B.K+、Fe2+、H+、NO3- |
| C.Mg2+、SO42-、SiO32-、H+ | D.NH4+、Al3+、Cl-、NO3- |