请回答下列问题。
苯佐卡因是一种医用麻醉药品,学名对氨基苯甲酸乙酯。用芳香烃A为原料合成苯佐卡因E的路线如下:
请回答:
⑴写出结构简式 B ▲ C ▲ 。
⑵写出反应类型 ① ▲ ② ▲ 。
⑶化合物D经聚合反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域。写出该聚合反应的化学方程式:
▲ 。
⑷下列化合物中能与E发生化学反应的是 ▲ 。
a. HCl b. NaCl c. Na2CO3 d. NaOH
⑸除 、
、 、
、 外,符合下列条件的化合物E的同分异构体有 ▲ 种。
外,符合下列条件的化合物E的同分异构体有 ▲ 种。
i. 为1,4—二取代苯,其中苯环上的一个取代基是氨基;
ii. 分子中含 结构的基团
结构的基团
为应对环境污染,使得对如何减少煤燃烧和汽车尾气中各种含碳、氮、硫等气体的排放,及有效地开发利用碳资源的研究显得更加紧迫。
(1)为减少煤燃烧中废气的排放,常将煤转化为清洁气体燃料。请写出焦炭与水蒸气高温下反应的化学方程式:。
(2)选择适当的催化剂在高温下可将汽车尾气中的 CO、NO转化为无毒气体。
已知:①2CO(g)+O2(g)=2CO2(g)∆H1="-566" kJ∙mol-1
②2NO(g)+2CO(g) ⇋N2(g)+ 2CO2(g)∆H2="-746" kJ∙mol-1
则反应N2(g)+ O2(g)= 2NO(g)的∆H=kJ∙mol-1。
(3)在一定温度下,向1L密闭容器中充入0.5 mol NO、2 mol CO,发生上述反应②,
20s反应达平衡,此时CO的物质的量为1.6 mol。在该温度下反应的平衡常数K=。
(4)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用以CO2和H2O为原料制备HCOOH和O2的原理示意图。催化剂b表面发生的电极反应式为_____________________。
(5)氮氧化物进入水体可转化为NO3─,电化学降解法可用于治理水中NO3─的污染。原理如图所示。
电源正极为(填“A”或“B”),若电解过程中转移了0.4mol电子,则处理掉的NO3─为g。
合成有机玻璃树脂 和高聚物H的合成路线如下:
和高聚物H的合成路线如下:
已知:
RCOOR′+ R″OH RCOOR″ + R′OH (R、R′、R″代表烃基)
RCOOR″ + R′OH (R、R′、R″代表烃基)
CH2=CH—CH=CH2+CH2=CH2

试回答:
(1)E中官能团的名称是。
(2)C到D的反应类型是,D到E反应的“一定条件”是。
(3)下列说法正确的是(选填字母)。
| A.乙可使Br2的CCl4溶液褪色 |
| B.G与乙二醇互为同系物 |
| C.D的核磁共振氢谱有4组峰,且峰面积之比为3:1:1:1 |
| D.生成有机玻璃树脂和高聚物H均为加聚反应 |
(4)B到C的化学方程式是。
(5)乙的同分异构体中含有酯基的有种,写出其中能发生银镜反应的一种同分异构体的结构简式。
(6)生成高聚物H的化学方程式是。
废旧显示屏玻璃中含SiO2、Fe2O3、CeO2、FeO等物质。某课题小组以此玻璃粉末为原料,制得Ce(OH)4和硫酸铁铵矾[Fe2(SO4) 3·(NH4) 2SO4·24H2O],流程设计如下: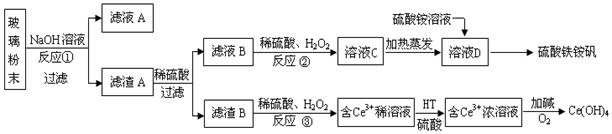
已知:Ⅰ.酸性条件下,铈在水溶液中有Ce3+、Ce4+两种主要存在形式,Ce4+有较强氧化性;
Ⅱ.CeO2不溶于稀硫酸,也不溶于NaOH溶液。
回答以下问题:
(1)反应①的离子方程式是。
(2)反应②中H2O2的作用是。
(3)反应③的离子方程式是。
(4)已知有机物HT能将Ce3+从水溶液中萃取出来,该过程可表示为:
2Ce3+ (水层)+ 6HT(有机层) 2CeT3 (有机层)+ 6H+(水层)
2CeT3 (有机层)+ 6H+(水层)
从平衡角度解释:向CeT3 (有机层)加入H2SO4 获得较纯的含Ce3+的水溶液的原因是。
(5)硫酸铁铵矾[Fe2(SO4) 3·(NH4) 2SO4·24H2O]广泛用于水的净化处理,其净水原理用离子方程式解释是。
(6)相同物质的量浓度的以下三种溶液中,NH4+的浓度由大到小的顺序是。
a.Fe2(SO4) 3·(NH4) 2SO4·24H2O
b.(NH4) 2SO4
c.(NH4) 2CO3
碳和氮的化合物与人类生产、生活密切相关。
(1)C、CO、CO2在实际生产中有如下应用:
a.2C + SiO2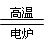 Si + 2CO b.3CO + Fe2O3
Si + 2CO b.3CO + Fe2O3 2Fe + 3CO2
2Fe + 3CO2
c.C + H2O CO + H2 d.CO2 + CH4
CO + H2 d.CO2 + CH4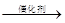 CH3COOH
CH3COOH
上述反应中,理论原子利用率最高的是。
(2)有机物加氢反应中镍是常用的催化剂。但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为搞清该方法对催化剂的影响,查得资料: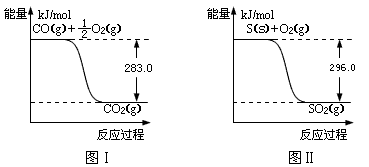
则:① 不用通入O2氧化的方法除去CO的原因是。
② SO2(g) + 2CO(g) =" S(s)" + 2CO2(g) △H =。
(3)汽车尾气中含大量CO和氮氧化物(NO )等有毒气体。
)等有毒气体。
①活性炭处理NO的反应:C(s)+2NO(g) N2(g)+CO2 (g) ∆H=-a kJ·mol-1(a>0)
N2(g)+CO2 (g) ∆H=-a kJ·mol-1(a>0)
若使NO更加有效的转化为无毒尾气排放,以下措施理论上可行的是:。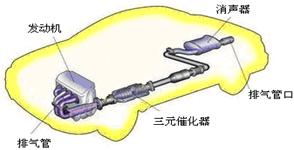

a.增加排气管长度 b.增大尾气排放口
c.添加合适的催化剂 d.升高排气管温度
②在排气管上添加三元催化转化装置,CO能与氮氧化物(NO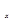 )反应生成无毒尾气,其化学方程式是。
)反应生成无毒尾气,其化学方程式是。
(4)利用CO2与H2反应可合成二甲醚(CH3OCH3)。以KOH为电解质溶液,组成二甲醚空气燃料电池,该电池工作时其负极反应式是。
(5)电解CO制备CH4和W,工作原理如图所示,生成物W是,其原理用电解总离子方程式解释是。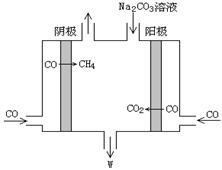
(15分)二氧化碳的过度排放会引发气候问题,而进行有效利用则会造福人类,如以CO2和NH3为原料合成尿素。经研究发现该反应过程为:
①CO2(g)+2NH3(g) NH2COONH4(s)△H1
NH2COONH4(s)△H1
②NH2COONH4(s) CO(NH2)2(s)+H2O(g)△H2>0
CO(NH2)2(s)+H2O(g)△H2>0
请回答下列问题:
(1)研究反应①的平衡常数(K)与温度(T)的关系,如图1所示,则△H1____0。(选填“>”、“<”或“=”)。
(2)有体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如图2所示,现将3molNH3和2molCO2放入容器中,移动活塞至体积V为3L,用铆钉固定在A、B点,发生合成尿素的总反应如下:
CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)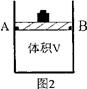
测定不同条件、不同时间段内的CO2的转化率,得到如下数据:
| CO2的转化率T(℃) |
10min |
20min |
30min |
40min |
| T1 |
30% |
65% |
75% |
75% |
| T2 |
45% |
50% |
a1 |
a2 |
①T1℃下,l0min内NH3的平均反应速率为__________。
②根据上表数据,请比较T1_________T2(选填“>”、“<”或“=”);T2℃下,第30min时,a1=________,该温度下的化学平衡常数为_________。
③T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人3molCO2,此时v(正)_____v(逆)(选填“>”、“<”或“=”),判断的理由是______。
(3)请在下图中补画出合成氨总反应2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)过程中能量变化图,并标明中间产物〔NH2COONH4(s)〕、生成物CO(NH2)2(s)+H2O(g)〕。
CO(NH2)2(s)+H2O(g)过程中能量变化图,并标明中间产物〔NH2COONH4(s)〕、生成物CO(NH2)2(s)+H2O(g)〕。