t℃时,水的Kw=10-12。则该温度 25℃(填“>”“<”或“=”),其理由是:
⑴将此温度下pH = 11的NaOH与pH=" 1" 的HCl等体积混合,混合后溶液pH= ;
⑵将此温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合:
①若所得混合液为中性,则a:b =
②若所得混合液的pH=2,则a:b =
⑶①常温下将pH=2的硫酸升温到该温度时,pH=
②将常温下pH=12的NaOH溶液升温到该温度时,pH=
T、X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增。已知:
①W的原子序数为29,其余的均为短周期主族元素;
②T原子所处的周期数、族序数分别与其原子序数相等;
③X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同;
④Z的基态原子价电子排布为ns2npn+2;
⑤在该元素所在周期中,Q的基态原子的第一电离能最小;
⑥R的单质常温常压下是气体,其基态原子的M层上有1个未成对的p电子;
(1)X、Y、Q三种元素的电负性由大到小的顺序是(用元素符号表示)。
(2)Y的氢化物分子间能形成氢键,R的氢化物分子间不易形成氢键,原因是。
(3)W的基态原子的外围电子排布式为,该元素与元素X、Y能形成的[W(XY)4]2-离子中,含有的化学键是。
a.离子键b.极性键c.非极性键d.配位键
(4)T、X、Z三种元素组成的一种化合物M是新装修居室中常见的有害气体,它的分子式为XT2Z,分子空间构型为平面三角形,则该分子中中心原子采取杂化,1molM分子中σ键和π键的个数比为。
(5)X与Y原子结合形成的X3Y4晶体,其晶体结构与金刚石类似,但硬度比金刚石大,请解释原因是。
(6)WR的晶胞结构如图所示,阴离子周围最近的阳离子有个 ;
;
WR晶体的密度为ag·cm-3,则晶胞的体积是(只要求列出计算式)。
二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g) CH3OH(g)△H1=-90.7kJ·mol-1
CH3OH(g)△H1=-90.7kJ·mol-1
②2CH3OH(g) CH3OCH3(g) +H2O(g)△H2=-23.5kJ·mol-1
CH3OCH3(g) +H2O(g)△H2=-23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g)△H3=-41.2kJ·mol-1
CO2(g)+H2(g)△H3=-41.2kJ·mol-1
(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为。
| A.加入某物质作催化剂 | B.加入一定量CO |
| C.反应温度降低 | D.增大容器体积 |
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2.4 mol/L,5 min后达到平衡,CO的转化率为50%,则5 min内CO的平均反应速率为;若反应物的起始浓度分别为:c(CO)=4 mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2 mol/L,a=mol/L。
(3)催化反应室中总反应3CO(g)+3H2(g) CH3OCH3(g)+CO2(g)的△H=;830℃时反应③的K=1.0,则在催化反应室中反应③的K1.0(填“>”、“<”或“=”)。
CH3OCH3(g)+CO2(g)的△H=;830℃时反应③的K=1.0,则在催化反应室中反应③的K1.0(填“>”、“<”或“=”)。
(4)二甲醚的燃烧热为1455 kJ·mol-1,则二甲醚燃烧的热化学方程式为
。
(5)“二甲醚燃料电池”是一种绿色电源,其工作原理如图所示。b电极是极,写出a电极上发生的电极反应式。
已知5种元素的原子序数的大小顺序为C > A > B > D > E, A、C同周期,B、C同主族,A与B形成的离子化合物A2B中,所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子分子,请回答:
(1)写出元素符号:AC
(2)写出电子式:D元素的单质;B与E形成的化合物;
(3)用电子式表示离子化合物A2B的形成过程
T℃时,将3mol气体A和1mol气体B通入容积为2L且固定不变的密闭容器中,发生如下反应:3A(g)+B(g)  xC (g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写下列空白:
xC (g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写下列空白:
⑴x=;
⑵若向原平衡混合物的容器中再充入amol C ,在T℃达到新的平衡,此时B的物质的量为n(B)=mol;
⑶保持温度和容积不变,对原平衡混合物中三者的物质的量作如下调整,可使平衡向右移动的是;
A.均减半 B.均加倍 C.均增加0.4mol D.均减少0.4mol
⑷若上述可逆反应的热化学方程式为:3A(g)+B(g)  xC (g) ΔH=" -QkJ/mol" (Q>0)
xC (g) ΔH=" -QkJ/mol" (Q>0)
①若可逆反应达到平衡后升高体系温度,正反应速率(填“增大”、“减小”或“不变”,平衡将。(填“左移”、“右移”或“不移动”)
②若可逆反应达到平衡后增大压强,则体系温度将;(填“升高”、“降低”或“不变”)
②可逆反应达到平衡后,加入A,则ΔH。(填“变大”、“变小”或“不变”)
(7分)乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。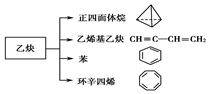
完成下列各题:
(1)正四面体烷的分子式为________,其二氯取代产物有________种。
(2)关于乙烯基乙炔分子的说法错误的是________。
a.能使酸性KMnO4溶液褪色 b.1mol乙烯基乙炔能与3molBr2发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式。
(4)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例)________、________。