高铁酸盐(如K2FeO4)是一种高效绿色氧化剂,可用于饮用水和生活用水的处理。从环境保护的角度看,制备高铁酸盐较好的方法为电化学法。
(1)电化学法制备高铁酸钠采用铁片作阳极,NaOH溶液作为电解质溶液,其电流效率可达到40%。写出阳极产生高铁酸钠的电极反应方程式: 。
(2)铁丝网电极是更理想的阳极材料,相同条件下,可将电流效率提高至70%以上,原因是 。研究亦发现,铁电极在某一电压范围内会产生氧气使阳极表面生成Fe2O3膜而“钝化”。写出产生O2的电极反应方程式: 。
(3)FeO42—易与水4h生成絮状氢氧化铁,也会影响高铁酸盐的产率。若以铁丝网为阳极,在中间环节(对应图中4h后)过滤掉氢氧化铁,反应过程中FeO42—浓度以及电流效率随时间的变化如图1中实线所示(图中曲线是每隔1h测得的数据)。图中虚线部分对应于没有过滤氢氧化铁而连续电解的情况。下列判断正确的是 (填编号)
①过滤:掉氢氧化铁有利于获得较高浓度的高铁酸盐溶液
②过滤掉氢氧化铁对电流效率影响不大
③实验表明不过滤掉氢氧化铁,6h后电流效率几乎为0
(4)在相同的pH条件下,经过相同的反应时间,高铁酸盐的产率与温度关系如图2。
随温度升高,高铁酸盐产率先增大后减小的原因是 。
(5)人们还对用铁的氧化物作电极制备高铁酸盐进行了研究,例如以磁铁矿多孔电极制备高铁酸盐,该研究方向的价值有 (至少答一点)。
从某废触媒[主要成分为活性炭、ZnO、FeO、(CH3COO)2Zn]中制取醋酸锌晶体的实验步骤如下:
(1)浸取时,在三口烧瓶中加入废触媒及稀醋酸,给三口烧瓶加热并同时开动搅拌器的目的是。
(2)若先将废触媒在马弗炉中通氧气500℃处理一段时间,浸出率会大大提高,其原因是。抽滤时用的硅酸盐质仪器有和。
(3)流程图中加入H2O2的目的是。
(4)所得晶体(CH3COO)2Zn·2H2O热重分析(TG/%=固体样品的剩余质量/固体样品的起始质量),文献表明分解分三个阶段,在200°C以下脱去两分子结晶水,形成的(CH3COO)2Zn在242°C熔融,370°C完全分解为ZnO同时生成CO2及一种含氧衍生物(核磁共振氢谱只有1组峰)。(CH3COO)2Zn分解生成氧化锌的反应方程式为。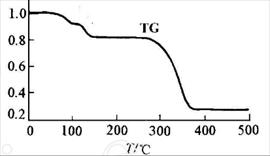
实验室用MnO2、KOH及KClO3为原料制取高锰酸钾的实验流程如下:
(1)熔融时需用铁坩埚和铁制搅拌棒而不能用玻璃仪器,其原因是。
(2)熔融时,MnO2转化为K2MnO4,KClO3转化为KCl,其反应的化学方程式为。
(3)几种物质的溶解度曲线如图所示。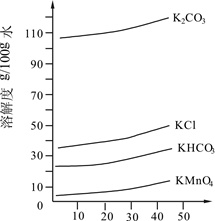
①歧化时,通入CO2至pH为10~11,K2MnO4绿色溶液转化为KMnO4和MnO2。其反应的离子方程式为。
②歧化时不能通入过量CO2的原因是。
③通入CO2后,用玻璃棒蘸取溶液点于滤纸上,观察到,证明歧化反应已发生。
④歧化后得到KMnO4晶体的操作依次为过滤、、及干燥。
(4)在此实验流程中可循环使用的物质的化学式为。
利用硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)生产铁基颜料铁黄(FeOOH)的制备流程如下: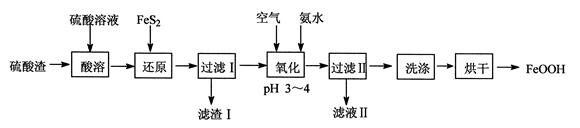
(1)“酸溶”时,Fe2O3与硫酸反应的化学方程式为。
(2)滤渣Ⅰ的主要成分是FeS2、S和(填化学式);Fe3+被FeS2还原的离子方程式为。
(3)“氧化”中,生成FeOOH的离子方程式为。
(4)滤液Ⅱ中溶质是Al2(SO4)3和(填化学式);“洗涤”时,检验铁黄表面已洗涤干净的操作是。
B.【实验化学】
水杨酸可用于制备解热镇痛药阿司匹林。重结晶纯化固体水杨酸的步骤如下:
步骤1:按图1所示装置,在圆底烧瓶中加入1.2 g粗水杨酸,10 mL 30%乙醇和磁子。接通冷凝水后,搅拌加热至沸,直到完全溶解。
步骤2:冷却后,加入活性炭,重新搅拌加热煮沸几分钟后,利用图2装置趁热过滤到锥形瓶中,并在短颈漏斗上盖好表面皿。
步骤3:盛滤液的锥形瓶用塞子塞好,自然冷却后再用冰水冷却,析出水杨酸晶体。
步骤4:用图3所示装置进行抽滤,用少量30%的乙醇洗涤。抽干后得到的晶体转移到表面皿上,放入干燥器中干燥。
步骤5:称量干燥后固体质量为0.81 g。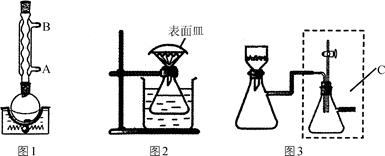
(1)步骤1中接通冷凝水时,冷水应从________(填“A”或“B”)端进。
(2)步骤2中“趁热过滤”的目的是______________________。
(3)步骤3中“自然冷却后再用冰水冷却”,而不直接用冰水浴冷却的目的是________。
(4)步骤4中C装置的作用是______________________________________。
(5)本次实验中,水杨酸的收率为________。确定最终产品是水杨酸的实验或方法是___________。
二氯化二硫(S2Cl2),常温下是一种黄红色液体,有窒息性,刺激性恶臭,熔点80℃,沸点135.6℃,在空气中强烈产生烟雾,遇水、醇即分解;它常用于橡胶的低温硫化和黏接剂,国防工业用作军用毒气。它的工业合成方法:将氯气通入到熔融的硫单质发生反应而制得。实验室用下列装置制取少量S2Cl2。
请回答下列问题:
(1)S2Cl2分子中各原子均达到8电子稳定结构,则它的结构式为。
(2)下列方法都可以制得氯气,其中符合装置A制取的有。
a、MnO2固体和浓HCl共热
b、KMnO4固体和浓HCl反应
c、KClO3固体和浓HCl反应
d、MnO2固体、NaCl固体和浓硫酸共热
(3)装置A中用恒压分液漏斗而不用普通分液漏斗的原因是。
(4)B中饱和食盐水的作用,装置C中的试剂是 。
(5)S2Cl2遇水强烈反应产生烟雾,其产物中有一种气体能使品红溶液褪色,加热后又恢复原状,且反应过程中只有一种元素化合价发生变化,写出该反应的化学方程式,其氧化剂与还原剂物质的量之比为。
(6)从安全和环保方面考虑,补全F方框内剩下的装置并注明装置中的药品。画图时,仪器可以简化,如下列仪器可以分别表示为: