在一定条件下,1 mol某气体若被O2完全氧化放热98.0 kJ,现有2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为
(注:某反应物的转化率=该反应物转化(消耗)的物质的量÷该反应物起始的物质的量×100%)
根据下列实验分别指出A、B、C、D、E各是什么物质。A____,B____,C____,D____,E____。
1mol某烃A,充分燃烧可以得到8 molCO2和4molH2O。烃A可通过如下图的各个反应得到各种化合物和聚合物:
(1)以上11个反应中,属于消去反应的有____个(填数字),它们分别是,由C→A,________(填写由x→y),写出其反应方程式。
(2)化合物的结构简式:
A是____,D是____,E是____,G是____。
假设双氧水(H2O2)是比碳酸还弱的二元酸。</PGN0031A.TXT/PGN>
(1)双氧水电离的方程式为___ _。
(2)若CO2与Na2O2不发生反应,而潮湿的CO2可与Na2O2反应,则该反应的化学方程式为:__ __。
Zn+2MnO2+2NH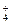 ===Zn2++Mn2O3+2NH3+H2O
===Zn2++Mn2O3+2NH3+H2O
(1)试写出干电池放电时的正、负电极反应式:正极:___________负极:___________
干电池用久了就会变软,其原因是____________________________________________。
(2)正极反应中,前后经历了下列两个反应:
2NH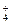 +2e-===2NH3+H2
+2e-===2NH3+H2
2MnO2+H2===Mn2O3+H2O
如果正极反应没有MnO2的参与,干电池将难以持续稳定工作。试说明理由。
(3)在通电10 min的时间内参加反应的MnO2质量约为多少?外电阻消耗的电能是多少?
(4)许多国家对废旧电池进行回收,从保护环境和节约能源解释为什么要回收废旧电池。
阳极反应式:2CO+2CO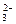
 4CO2+4e-
4CO2+4e-
阴极反应式: ,总电池反应式: 。