已知电离平衡常数:H2CO3>HClO>HCO3—,下列有关叙述中,正确的是:
①若KI溶液中混有Br-,加入足量FeCl3溶液,用CCl4萃取后,取无色的水层并加入AgNO3溶液,有淡黄色沉淀生成。
②向FeI2溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl2===2Fe3++2Cl-
③向NaClO溶液中通入少量二氧化碳的离子反应方程式:
2ClO-+CO2+H2O===2HClO+CO32—
④海水提溴过程中,用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为
3 Br2+6 CO32-+3H2O="5" Br-+ BrO3-+6HCO3-
| A.②④ | B.①③ | C.②③ | D.①④ |
实验室需480 mL 1.0 mol/L的NaOH溶液,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是:
| A.称取氢氧化钠20.0 g |
| B.定容时俯视观察刻度线 |
| C.移液时,对用于溶解氢氧化钠的烧杯没有进行冲洗 |
| D.移液用玻璃棒引流时,玻璃棒下端靠在容量瓶刻度线上方 |
已知常温下,AgBr的Ksp=4.9×10-13 mol2·L-2、AgI的Ksp=8.3×10-17 mol2·L-2下列说法正确的是:
| A.常温下AgI水溶液中,Ag+和I-浓度的乘积是一个常数 |
| B.常温下,在任何含AgI固体的溶液中,c(Ag+)=c(I-)且Ag+与I-浓度的乘积等于8.3×10-17mol2·L-2 |
| C.常温下,将1mL 1.0×10-2 mol/L的KI与AgNO3溶液等体积混合,则生成AgI沉淀所需AgNO3溶液的最小浓度为3.32×10-14 mol/L |
| D.向AgI饱和溶液中加入AgBr固体,c(I-)不变,Ksp值不变 |
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
A.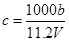 |
B.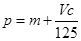 |
| C.n="m+17V" c | D.5/3 m< 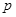 < <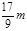 |
如图判断,下列说法正确的是
| A.装置Ⅰ和装置Ⅱ中负极反应均是Fe-2e-===Fe2+ |
| B.装置Ⅰ和装置Ⅱ中正极反应均是O2+2H2O+4e-===4OH- |
| C.装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动 |
| D.放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的pH均增大 |